Обязательный тур (десятый класс решения)
Задача 10-1
Индивидуальное соединение, при нагревании
которого выделяется NO2 может быть нитратом
либо нитритом металла. Поскольку жидких
продуктов не образовалось, это не
кристаллогидрат. При его нагревании могут
образовываться либо оксид металла, либо чистый
металл. Оценим эквивалентную массу металла M(M)/n (n
– его валентность) для всех случаев.
Случай 1. Исходное вещество - нитрат, при
нагревании образуется металл.
M(M)/M(M(NO3)n) = 0,63/1,00
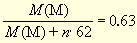
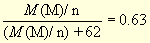 ,
,
откуда M(M)/n = 105,6. Такого металла нет. Но
взвешивание произведено с погрешностью, поэтому
необходимо оценить диапазон эквивалентной массы
металла. Максимальной она будет, если масса
исходного вещества окажется 0,99 г (нижний предел
истинной массы) при массе продукта 0,64 г (верхний
предел истинной массы). Тогда соотношение в
правой части уравнения становится равным 0,646, а M(M)/n
= 113. Минимальной она будет, если масса исходного
вещества окажется 1,01 г (верхний предел истинной
массы) при массе продукта 0,62 г (нижний предел
истинной массы). Тогда соотношение в правой части
уравнения становится равным 0,614, а M(M)/n =
98,5. То есть, с учетом погрешности взвешивания
эквивалентная масса металла лежит в диапазоне
98-113. В этот диапазон укладывается серебро с
эквивалентной массой 107.
2AgNO3 = 2Ag + 2NO2 + O2.
Случай 2. Исходное вещество - нитрат, при
нагревании образуется оксид металла в той же
степени окисления. Для нахождения минимальной
эквивалентной массы
M(MOn/2)/M(M(NO3)n) = 0,62/1,01
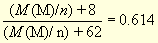 ,
,
откуда M(M)/n = 77,8. Аналогично максимальная
оценка дает M(M)/n = 90,7. Металлов с такими
эквивалентными массами, разлагающихся до
оксидов без изменения степени окисления металла
и при этом не радиоактивных, нет.
Случай 3. Исходное вещество - нитрит, при
нагревании образуется металл. Для нахождения
минимальной эквивалентной массы
M(M)/M(M(NO2)n) = 0,62/1,01
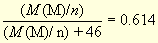 ,
,
откуда M(M)/n = 73. Аналогично максимальная
оценка дает M(M)/n = 84. Металлов с такими
эквивалентными массами, нитриты которых
разлагались бы с образованием металла, нет.
Случай 4. Исходное вещество - нитрит, при
нагревании образуется оксид металла в той же
степени окисления. Для нахождения минимальной
эквивалентной массы
M(MOn/2)/M(M(NO2)n) = 0,62/1,01
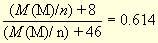
откуда M(M)/n = 52,4. Аналогично максимальная
оценка дает M(M)/n = 61,5. Под все условия
задачи ни один металл не подходит (Cd и РЗМ,
подходящие по химическим свойствам, не образуют
темно-серых оксидов).
Кроме четырех рассмотренных случаев возможны
нитраты металлов, разлагающиеся с повышением
степени окисления металла. К таким нитратам
относятся, в частности, CuNO3, Mn(NO3)2.
Так же ведут себя Fe(NO3)2 и Ce(NO3)3,
но образующиеся при этом оксиды не имеют
темно-серой окраски. Проверим первые два
соединения на соответствие условиям задачи.
CuNO3 = CuO + NO2
M(CuO)/M(CuNO3) = 80/126 = 0,635, что вполне
укладывается в диапазон 0,614 ч 0,646, получаемый с
учетом погрешностей при взвешивании. То есть CuNO3
вполне может быть исходным соединением.
Mn(NO3)2 = MnO2 + 2NO2
M(MnO2)/M(Mn(NO3)2) = 87/179 = 0,486, что не
укладывается в диапазон 0,614-0,646. То есть Mn(NO3)2
не может быть исходным соединением.
Таким образом, порошок А - либо AgNO3, либо CuNO3.
Задача 10-2
- Бром (от греческого "бромос" – зловонный).
Название "мурий" не прижилось, т.к. муриевой
кислотой (acidum muriaticum) называли соляную кислоту, из
которой был получен в свое время хлор (т.е.
название не приняли во избежание путаницы хлора
и брома).
- А. Балар. Цитата Ю. Либиха "Это не Балар
открыл бром, а бром открыл для нас Балара!" ICl –
имеет близкую молярную массу.
- Кто не знает историю химии, то "выйти" на
бром можно при ответе на этот вопрос.