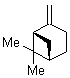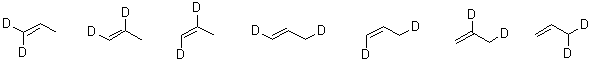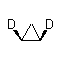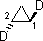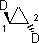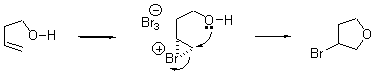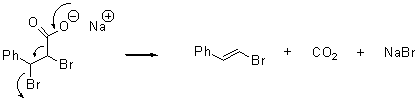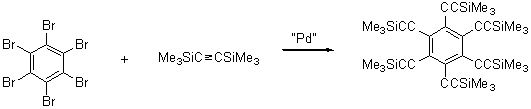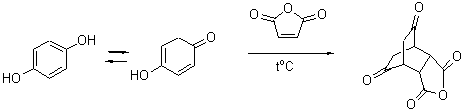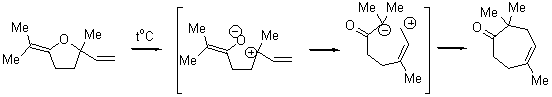|
Материалы для аспирантов:Вступительный тест по органической химии
Ответы на задачи вступительного теста для аспирантов.
1.
2.
- (S)-Иодобутан-1-ол;
- (R,S)-1,2-дихлоропропан;
- (1S)-хлоро-(2R )-метилциклопропан.
3.
3.1
3.2
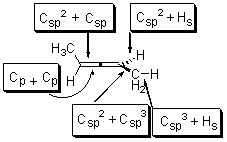
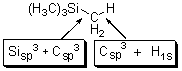
4.
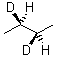
4.1.C3H4D2 . Среди соединений с
такой формулой могут быть
а) алифатические непредельные соединения и
б) насыщенные карбоциклы.
а)
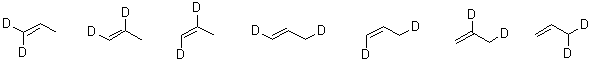 |
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
| 1,1 |
(E)-1,2- |
(Z)-1,2- |
(E)-1,3- |
(Z)-1,3 |
2,3 |
3,3-дидей-
теро - про-
пен |
б)
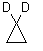 |
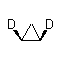 |
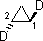 |
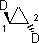 |
8
1,1- |
9
(Z)-1,2 |
10
(1R, 2R) -дидейтероциклопропан |
11
(1R,2R) -дидейтероциклопропан |
Всего 11 изомеров.
4.2. C3H6O. Такую формулу могут иметь а)
карбонильные соединения,
б) ненасыщенные алифатические соединения с
простыми эфирными и спиртовыми функциями,
в) насыщенные карбоциклы и
г) насыщенные гетероциклы.
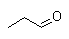 |
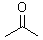 |
 |
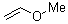 |
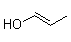 |
 |
 |
1 (а)
Пропионовый альдегид |
2(а)
Ацетон |
3,(б) Аллиловый
спирт; пропен-3-ол |
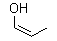
4,(б) Винилметиловый
эфир |
5, (б) ( Е)-
Проп-1-ен-1-ол |
6,(б) (Z)-
Проп-1-ен-1-ол |
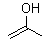
7,(б) Проп-1-ен-2-ол |
Последние три соединения легко
перегруппировываются в соответствующиие
карбонильные соединения, но все они стабильны в
виде производных, таких как простые и сложные
эфиры, элементоорганические производные и др.
Всего 11 изомеров.
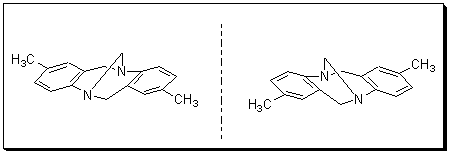
5.1
Соединение 5.1 хирально, существует в виде двух
энантиомеров, что следует из несовместимости
приведенной формулы и ее зеркального отражения.
Наиболее употре-бительное название – основание
Трегера.
5.2.Приведенное производное циклопропена
хирально. Известны обе энантиомерные фор-мы: ( R)-
и (S)- .
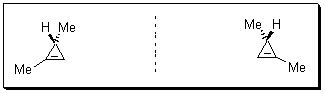
( R )-1,3-диметилциклопропен ( S
)-1,3-диметилциклопропен
5.3.
2,4,6-Триметил-3,5-диэтилгептан существует в виде
двух мезо- и двух энантиомерных форм:
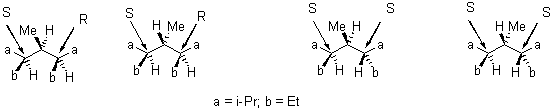
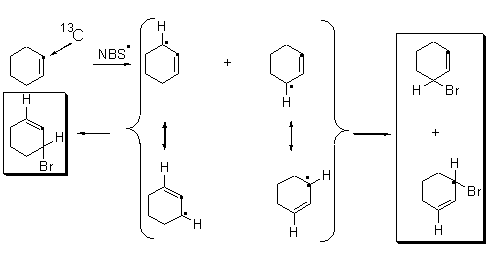
6. Аллильное бромирование в этой
реакции приведет к трем изомерным
3-бромоциклогек-сенам, различающимся
относительным положением брома и изотопной
метки 13С:
7.
7.1 Вода – более сильная кислота, чем
т-бутанол: рКа т-BuOH = 18, рКа H2O = 15.7.
7.2 NH4+ - более сильная кислота (рКа
= 9.24), чем MeOH (рКа = 15.5).
7.3.Этанол – более сильная кислота (рКа = 15.9),
чем пиперидин (рКа = 38).
8.
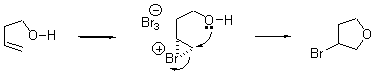
10.
10.1 Возможны различные синтетические подходы к
желаемому 1-галогенолефину. Среди них -
дегалогенодекарбоксилирование солей a, b
-дигалогеноалкановых кислот (реакция
Эрленмейера) и др.
Натриевая соль 2,3-дибромгидрокоричной кислоты,
легко доступная в результате бромирования
коричной кислоты и последующей нейтрализации,
способна претерпевать
дебромодекарбоксилирование при умеренном
нагревании (например, при нагревании в кипящем
четыреххлористом углероде). Это превращение a,b-
дигалогенопропионовых кислот используется как
общий метод синтеза 1-галогенолефинов.
Аналогичное дегалогено-декарбоксилирование
солей b-галогенопропионовых кислот или их более
сложных производных приводит к соответствующим
олефинам.
Следует отметить, что b-галогено- или
a,b-дигалогенокислоты отличаются более высокой
термической стабильностью.
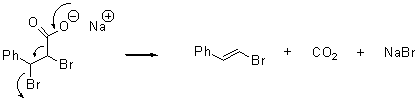
10.2
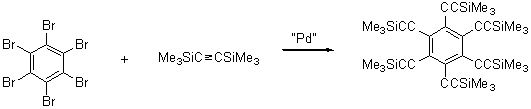
11.
11.1
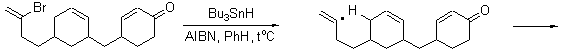
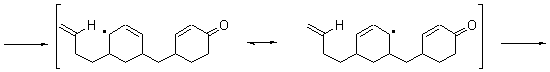
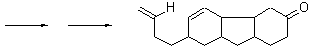
11.2
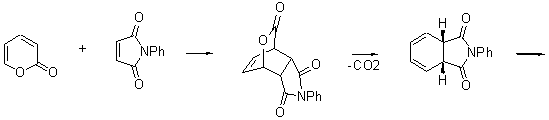
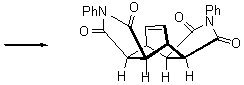
11.3
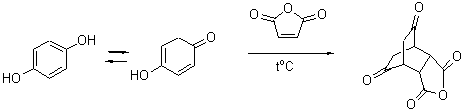
11.5
Аддукт состава 1:1 образуется с
количественным выходом:
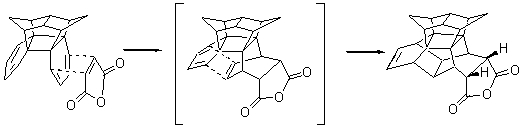
12.
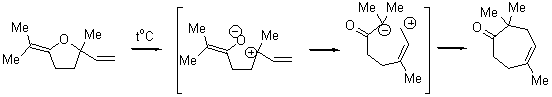
|