


Ткани и органы. Кровь
Кислотно-основной баланс
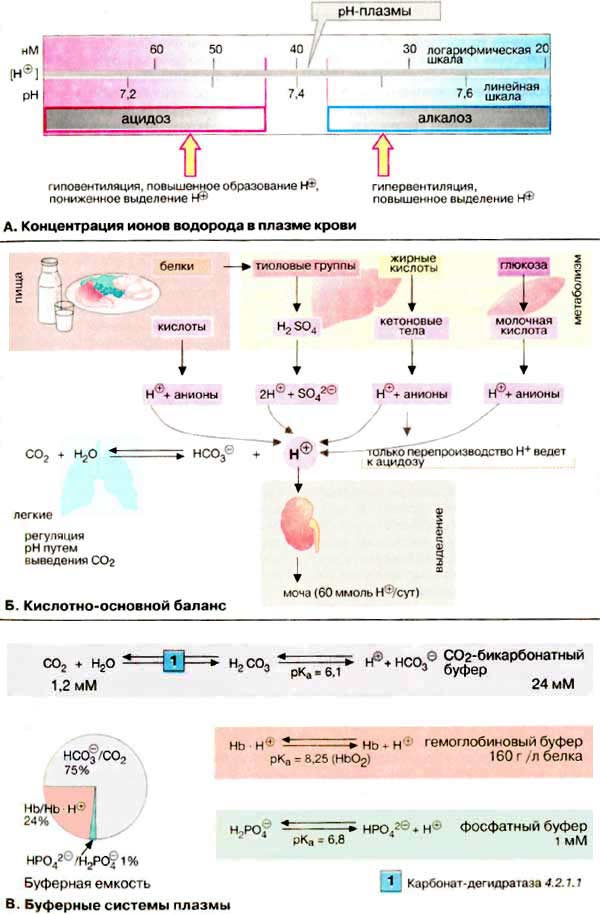 А. Концентрация ионов водорода в
плазме крови
А. Концентрация ионов водорода в
плазме крови
Концентрация ионов Н+ в
плазме и в межклеточном пространстве составляет около 40 нМ. Это соответствует
величине рН 7,40. рН внутренней среды организма должен поддерживаться
постоянным, так как существенные изменения концентрации прогонов не совместимы с
жизнью.
Постоянство величины рН поддерживается буферными системами
плазмы (схема В), которые могут компенсировать
кратковременные нарушения кислотно-основного баланса (см. с. 36).
Длительное рН-равновесие поддерживается с помощью продукции и удаления протонов.
При нарушениях в буферных системах и при несоблюдении кислотно-основного баланса,
например в результате заболевания почек или сбоев в периодичности дыхания из-за
гипо- или гипервентиляции, величина рН плазмы выходит за допустимые
пределы. Уменьшение величины рН 7,40 более, чем на 0,03 единицы, называется
ацидозом, а повышение — алкалозом
Б. Кислотно-основной
баланс
Происхождение протонов.
Существуют два источника протонов — свободные кислоты пищи и серосодержащие
аминокислоты белков, полученные с пищей кислоты, например лимонная,
аскорбиновая и фосфорная, отдают протоны в кишечном тракте (при щелочном рН). В
обеспечение баланса протонов наибольший вклад вносят образующиеся при
расщеплении белков аминокислоты метионин и цистеин. В печени атомы
серы этих аминокислот окисляются до серной кислоты, которая диссоциирует на
сульфат-ион и протоны.
При анаэробном гликолизе в мышцах и
эритроцитах глюкоза превращается в молочную кислоту (см. с. 330),
диссоциация которой приводит к образованию лактата и протонов. Образование
кетоновых тел — ацетоуксусной и 3-гидроксимасляной кислот — в
печени (см. с. 304) также приводит к освобождению протонов, избыток кетоновых
тел (при голодании, сахарном диабете) ведет к перегрузке буферной системы
плазмы и снижению рН (метаболический ацидоз; молочная кислота →
лактацидоз, кетоновые тела → кетоацидоз ). В нормальных условиях
эти кислоты обычно метаболизируют до СО2 и Н2О и не влияют
на баланс протонов.
Удаление протонов. В почках
протоны попадают в мочу за счет активного обмена на Na+-ионы. При
этом в моче протоны забу-фериваются, взаимодействуя с NH3 и фосфатом
(см. с. 318).
В. Буферные системы
плазмы
Наиболее важной буферной системой плазмы
является бикарбонатный буфер, состоящий из слабой угольной кислоты
(рК1 6,1) и ее кислого аниона бикарбоната. Угольная кислота
Н2СО3 находится в равновесии со своим ангидридом
СО2. Установление равновесия между обеими формами ускоряется
ферментом карбонат-дегидратазой ("карбоангидразой"). При рН плазмы
концентрации НСО3- и СО2 находятся в
соотношении 20/1. Растворенный в крови СО2 равновесно обменивается с
СО2 газовой фазы альвеол легких. Поэтому
НСО3-/СО2 -система является эффективной
открытой буферной системой. Ускоренное или замедленное дыхание изменяет
концентрацию СО2, что приводит к изменению рН плазмы
(дыхательный ацидоз или соответственно алкалоз). Таким образом,
легкие могут быстро и действенно влиять на рН плазмы без участия систем
удаления прогонов.
Белки плазмы и особенно
гемоглобин эритроцитов (см. с. 276) также способны присоединять протоны,
поддерживая постоянство рН. Определенный вклад в буферные свойства крови вносит
фосфат.