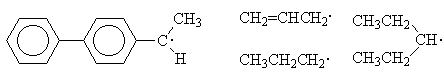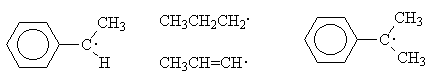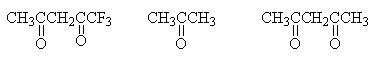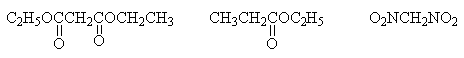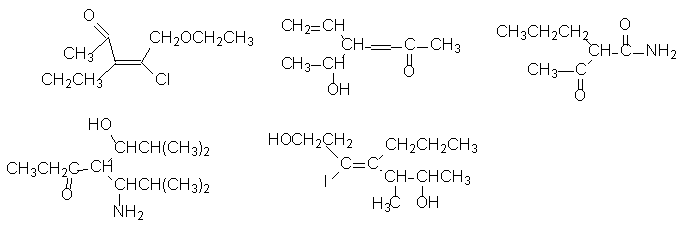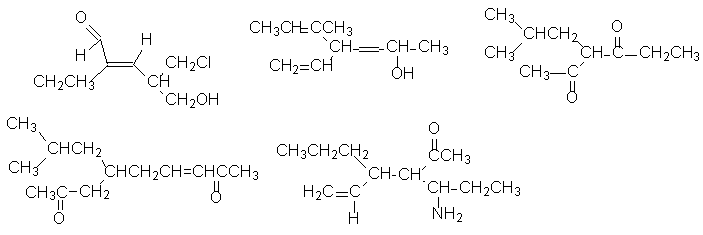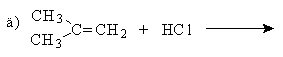|
Учебные материалы/ Зык Н.В., Белоглазкина Е.К., Подругина Т.А., Середа Г.А.
Cборник задач и упражнений по биоорганической химии
1. ОСНОВНЫЕ ПОНЯТИЯ ОРГАНИЧЕСКОЙ ХИМИИ
1.1. Расположите в ряд по увеличению
стабильности следующие радикалы:
а) 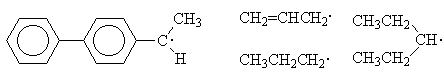
б) 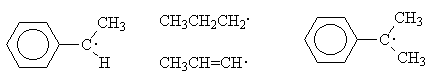
в) 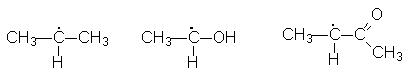
г) СHCl2., CH2Cl., CH3.
д) .СH2CH3, Cl-CH2-CH2.,
Cl-CH2-CH2-CH2.
1.2.Расположите следующие СН-кислоты в ряд по
увеличению кислотности. Для наиболее сильной
кислоты напишите соответствующее сопряженное
основание. Объясните его устойчивость с помощью
резонансных структур:
а) 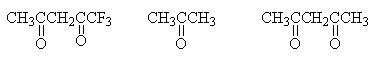
б) 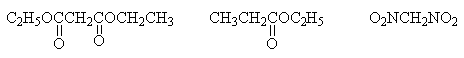
1.3.Сравните относительную основность:
а) воды и аммиака;
б) аммиака и амид-аниона;
в) ОН- и SH-;
г) анилина и циклогексиламина.
1.4.Расположите соединения в ряд по увеличению
кислотности. Объясните причину наблюдаемой
последовательности изменения кислотности:
а) H2O, C2H5ОН, фенол (C6H5-OH)
(ОН-кислоты);
б) этан, этилен, ацетилен (СН-кислоты);
в) метан, аммиак, вода, фтороводород;
г) AlH3, H2S, HCl, NaH;
д) уксусная кислота, ацетамид, метилацетат
(СН-кислоты);
е) этантиол, этанол, этиламин;
ж) пара-замещенные фенолы (ОН-кислоты):
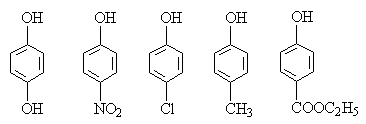 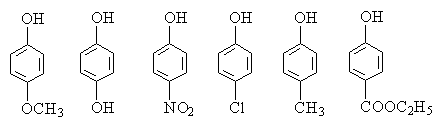
1.5.Расположите указанные анионысоединения в
ряд по увеличению основности. Объясните причину
наблюдаемой последовательности изменения
основности:
а) СH3-, NH2-, OR-, F-;
б) F-, Cl-, Br-, I-;
г) CH3-CH2-, CH2=CH-, HC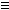 C-. C-.
1.6.Расположите соединения в ряд по увеличению
основности. Объясните причину наблюдаемой
последовательности изменения основности:
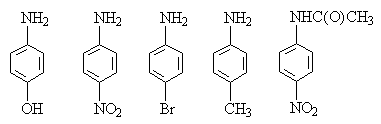
1.7. Назовите приведенные ниже соединения по
систематической номенклатуре:
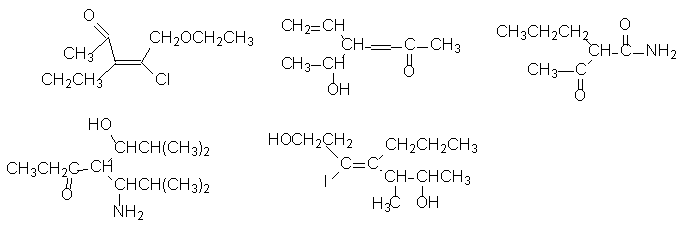
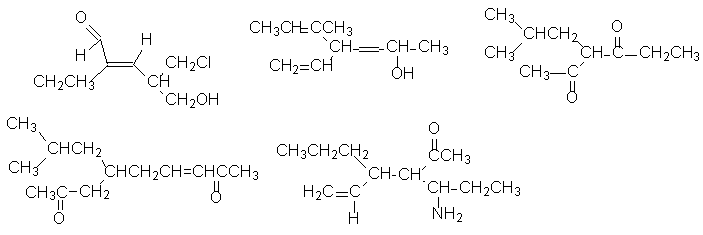
1.8. Напишите структурные формулы указанных
соединений (2 балла):
(Е)-3-Изопропил-4-хлоргексен-3-он-2;
4-Амино-2-винилпентен-2-овая кислота;
(Z)-4-амино-3-пропаргилпентен-3-он-2;
5-Аллил-2-гидроксигептин-3-диовая кислота.
1.9. Назовите следующие соединения по
рациональной номенклатуре:
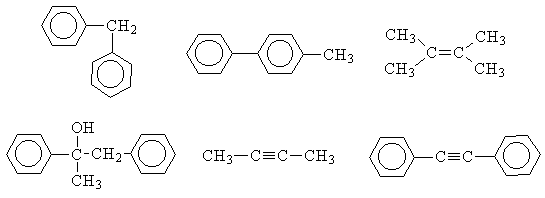
1.10. Напишите структурные формулы следующих
соединений:
а) метилвинилкарбинол;
б) трифторметилэтилен;
в) трихлоруксусная кислота;
г) фенилуксусная кислота;
д) триметилуксусная кислота;
е) метилизопропилацетилен.
1.11.Для каждой пары соединений предскажите,
какое соединение будет более растворимо в воде.
Укажите причину такого различия растворимости:
а) этанол и хлорэтан;
б) н-пропанол и н-пропантиол;
в) н-пентанол и 1,5-пентандиол;
г) пропионовая кислота и метилацетат;
д) н-пропилхлорид и н-пропиламин.
1.12.Напишите схемы реакций, которых можно
ожидать для взаимодействия следующих соединений
с AlCl3 (кислота Льюиса) и с H2SO4
(сильная протонная кислота):
а) диметиламин;
б) формальдегид;
в) ацетилен;
г) этанол;
д) диметилсульфид.
1.13.Напишите структурные формулы сопряженных
оснований для следующих соединений:
а) диметиловый эфир;
б) диэтиламин;
в) метилпропилсульфид;
г) пропионовый альдегид;
д) пентанон-3;
е)н-пропанол.
1.14.Предскажите, будет ли CF3CH2OH более
или менее сильной ОН-кислотой, чем СН3СН2ОН.
1.15.Предскажите, будет ли иодоформ (трииодметан)
более или менее сильной СН-кислотой, чем
хлороформ (трихлорметан).
1.16. Для каждого из приведенных соединений
изобразите структурную формулу, указав наиболее
кислый протон:
а) гидроксиуксусная кислота;
б) 1-нитропропан;
в) 3-меркаптопропанол-1;
г) 1,1-дибромпропанон-2.
1.17.Ион натрия, Na+ не проявляет свойств
сильного электрофила. Объясните этот факт. Будут
ли ионы Нg2+ и Cu2+ более или менее
электрофильны, чем Na+?
1.18.Допишите следующие уравнения, приведя
основной продукт, ожидаемый в каждом случае.
Классифицируйте каждый реагент как электрофил
или нуклеофил:
|