Влияние температуры на скорость химической реакции
Влияние температуры на количество столкновений молекул может быть показано с помощью
модели. В первом приближении влияние температуры на скорость
реакций определяется правилом Вант-Гоффа
(сформулировано Я. Х. Вант-Гоффом на основании
экспериментального изучения множества реакций):
|
В интервале температур от 0оС до 100оС при повышении температуры
на каждые 10 градусов скорость химической реакции возрастает в 2-4 раза:
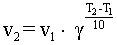
|
где g - tтемпературный коэффициент, принимающий значения от 2 до 4.
Хотите узнать, почему правило Вант-Гоффа - лишь первое
приближение к истине?
Объяснение зависимости скорости реакции от температуры было дано
С.Аррениусом.
К реакции приводит не каждое столкновение молекул реагентов, а только наиболее сильные столкновения.
Лишь молекулы, обладающие избытком кинетической энергии, способны к химической реакции.

С.Аррениус рассчитал долю активных (т.е. приводящих к реакции) соударений реагирующих частиц a,
зависящую от температуры: - a = exp(-E/RT).
и вывел уравнение Аррениуса для константы скорости реакции:
k = koe-E/RT
где ko и E dзависят от природы реагентов. Е - это энергия,
которую надо придать молекулам, чтобы они вступили во взаимодействие,
называемая энергией активации.
Хотите знать, почему?
Приложения
| 






