Медь и её соединения
Гидроксид меди
CuOH(г). Термодинамические свойства газообразного
гидроксида меди в стандартном состоянии в интервале температур 100 - 6000 К приведены в
табл. CuOH.
Молекулярные постоянные,
использованные для расчета термодинамических функций CuOH, приведены в табл. Cu.10. Тркула и Харрис [83TRK/HAR] исследовали спектры хемилюминесценции и
возбуждения лазером молекул CuOH и CuOD и заключили, что CuOH имеет изогнутую структуру (точечная группа Cs) в основном электронном состоянии 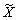 1A¢. Предположив для молекулы CuOHслегка вытянутый асимметричный волчок, авторы [83TRK/HAR] выполнили
вращательный анализ полосы (0,0,0) - (0,1,0) системы 1A²-
1A¢. Предположив для молекулы CuOHслегка вытянутый асимметричный волчок, авторы [83TRK/HAR] выполнили
вращательный анализ полосы (0,0,0) - (0,1,0) системы 1A²-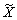 1A¢, определили вращательные постоянные и постоянные
центробежного растяжения для четырех изотопов и рассчитали эффективные
структурные параметры: r(Cu-O) = 1.774 ± 0.003 Å, r(O-H) = 0.933 ± 0.006 Å и ÐCu-O-H = 111 ± 1o. Произведение моментов инерции, приведенное в табл. Cu.10, вычислено по
вращательным постоянным для 63CuOH, A000 = 22.95, B000 = 0.39226 и C000 = 0.38482 см‑1[1].
Погрешностьрассчитанногозначения IAIBICсоставляет 1·10‑119г3·cм6.
1A¢, определили вращательные постоянные и постоянные
центробежного растяжения для четырех изотопов и рассчитали эффективные
структурные параметры: r(Cu-O) = 1.774 ± 0.003 Å, r(O-H) = 0.933 ± 0.006 Å и ÐCu-O-H = 111 ± 1o. Произведение моментов инерции, приведенное в табл. Cu.10, вычислено по
вращательным постоянным для 63CuOH, A000 = 22.95, B000 = 0.39226 и C000 = 0.38482 см‑1[1].
Погрешностьрассчитанногозначения IAIBICсоставляет 1·10‑119г3·cм6.
Частота деформационного колебания n2
рекомендована по работе Тркула и Харриса [83TRK/HAR]. Ее погрешность составляет 1 cм‑1. Кауфманидр. [85KAU/HAU] исследовали ИК спектры
в матрице и отнесли полосы 632.7 и 630.6 cм‑1 к Cu-Oвалентному колебанию 63CuOH и 65CuOH, соответственно. Значение n1 частоты, приведенное в табл. Cu.10, является округленной
величиной для 63CuOH; его погрешность оценена в 10 cм‑1. В работе
[85KAU/HAU] полоса при 727.1 cм‑1 была
отнесена к n2 частоте. Для колебательной частоты n3 рекомендовано характеристическое значение валентного колебания О-Н, ее
погрешность оценена в 200 cм‑1.
По аналогии с изоэлектронной CuFмолекулой (см. табл. Cu.4), можно ожидать для CuOHнесколько низколежащих синглетных и триплетных возбужденных состояний. CuF имеетблизкиенизколежащиеэлектронныесостоянияA1S+и B1P. Так как наблюденная в работе
[83TRK/HAR] полоса поглощения CuOHотнесена к электронному переходу 1A²-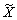 1A¢, величина энергии
1A²состояния
отнесена к двум синглетным низколежащим возбужденным состояниям этой молекулы с
погрешностью в 1000 cм‑1. Энергии двух триплетных состояний (см. табл. Cu.10) оценены с
погрешностью 3000 cм‑1[2].
1A¢, величина энергии
1A²состояния
отнесена к двум синглетным низколежащим возбужденным состояниям этой молекулы с
погрешностью в 1000 cм‑1. Энергии двух триплетных состояний (см. табл. Cu.10) оценены с
погрешностью 3000 cм‑1[2].
Термодинамические
функции CuOH(г)
вычислены в приближении "жесткий ротатор - гармонический осциллятор" по уравнениям (1.3) - (1.6), (1.9),
(1.10), (1.122) - (1.124),
(1.128), (1.130) и (1.168) - (1.170). Колебательно-вращательные парциальные
функции CuOHв возбужденных электронных
состояниях приняты такими же, как основного электронного состояния. Погрешности
рассчитанных термодинамических функций обусловлены в основном приближенным
характером расчета. Неточность в величинах энергий возбужденных электронных состояний
и пренебрежение эффектом центробежного искажения становятся заметными только
при высоких температурах. Суммарные погрешности составляют 0.2, 1 и 2 Дж×K‑1×моль‑1 в значениях Φº(T) при 298.15, 3000 и 6000 К.
Таблица термодинамических
функций CuOH(г)
публикуется впервые.
Константа равновесия CuОH(г) = Cu(г) + О(г) + H(г) вычислена по
значению DrH°(0) = 679.637 ± 15кДж×моль‑1, соответствующему принятой энтальпии образования
DfH°(СuОН, г, 0) = 120 ± 15 кДж×моль‑1 .
Величина основана на спектрофотометрических измерениях Булевич и Сагдена
[56BUL/SUG] (пламена Н2 + воздух, 1965-2380К, 31 точка) и Беляева и др. [78БЕЛ/ЛЕБ] (пламена СН4 + О2,
2155-2900К, 25 точек). В обеих работах определены температурные зависимости
константы равновесия СuОН(г) = Сu(г) + ОН(г), и по уравнению П
закона термодинамики вычислены значения DrH°0) = 247 ± 17 и 259 ± 13 кДж×моль‑1 (DfH°(СuОН) = 129 ± 17 и 116 ± 13 кДж×моль‑1, соответственно).
АВТОРЫ
Osina E.L. j_osina@mail.ru
Гусаров А.В. a-gusarov@yandex.ru
[1]Для 63CuOH, константы центробежного искажения были определены как : DJ = 6.5·10-7, DJK = 0.1·10-4 и DK = 0.9·10-8 см‑1.
[2]Результаты анализа систем B1A²-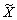 1A¢ и A1A²-
1A¢ и A1A²-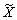 1A¢CuOH и CuOD в спектре лазорной флуоресценции [90JAR/FER, 91JAR/FER] находятся в хорошем
согласии с молекулярными постоянными CuOH, приведенными в табл. Cu.10.
1A¢CuOH и CuOD в спектре лазорной флуоресценции [90JAR/FER, 91JAR/FER] находятся в хорошем
согласии с молекулярными постоянными CuOH, приведенными в табл. Cu.10.
Версия для печати