VIII. Физика химических реакций
Химия, как всякая высокоразвитая наука, стала наукой высокого риска - в том смысле, что ее задачи сложны и не всегда могут быть решены современными методами, поэтому в научном поиске высока степень неудач, бесплодных затрат труда, времени и средств. Снизить степень риска можно лишь на основе глубокого понимания физики химических реакций - наиболее важной и элитарной части химической физики.
В основе физики химических реакций
лежат четыре динамики:
- молекулярная динамика и молекулярная
организация;
- энергетическая динамика (энергетическая
динамика в газах, миграция энергии в кластерах,
трансформация энергии в жидкостях,
энергетическая релаксация в твердых телах);
- химическая динамика (поверхности потенциальной
энергии, энергетика в химической динамике,
теория химических реакций);
- динамика углового момента и спиновая динамика.
Физика химических реакций - экспериментально-теоретическая наука, успехи ее закономерны, проблемы традиционно ясны (их анализ дан в работе24). На острие этой науки находится химическая динамика и ее главная часть - теория химических реакций.
Химическая динамика выросла из химической кинетики, которая в настоящее время является общехимической наукой: она вошла во все разделы химии и способствовала разработке универсальных кинетических критериев механизмов реакций.
Однако если химическая кинетика измеряет число химических событий, т.е. время между ними, то химическая динамика измеряет время самого события - движения реагентов по поверхности потенциальной энергии. И это центральное событие, вокруг которого обращается вся химия и которое составляет сердце химической реакции. Химическая динамика есть кардиограмма этого "химического" сердца.
Успехи теории химических реакций - особая богатая тема.67,68 Фактически она призвана решать две крупные задачи: построение поверхностей потенциальной энергии и расчет движения ядер реагентов в рассчитанных потенциальных полях (собственно динамика химического акта).
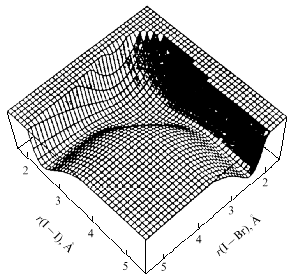
Обе задачи решаются в разных вариантах, на разных уровнях приближений, с разной степенью учета квантовости движения. В принципе сегодня для любой реакции можно построить потенциальные поверхности с любой степенью точности (при этом необходимо уметь сколь угодно сложную реакцию сводить к простой без потери физического и химического содержания с учетом возможностей современной вычислительной техники). Разработаны надежные методы расчета динамических траекторий движения реагентов на потенциальных поверхностях: метод классических траекторий (по законам классической механики Гамильтона-Ньютона-Лагранжа), полуклассических (учет квантовых эффектов через суперпозицию начальных квантовых состояний реагентов) и чисто квантовых траекторий (из решений уравнения Шредингера с получением вероятностей превращения реагентов по всем каналам - Д-матрицы, или матрицы рассеяния). Из совокупности траекторий рассчитываются константы скорости - канонические k(T) и микроканонические k(E), где Т и Е - температура и энергия. Два примера таких расчетов показаны на рис. 14 и 15.
 |
 |
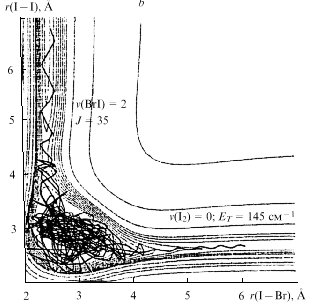
| Рис. 14. Поверхность потенциальной
энергии реакции Br + I2 |
|
 |
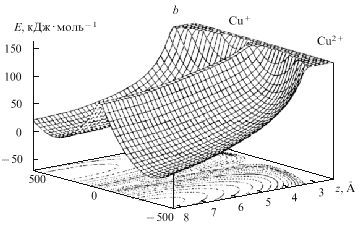 |
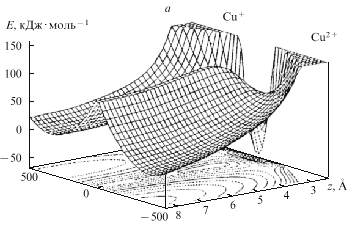
| Рис. 15. Поверхности свободной энергии
реакции Cu2+ |
|
Разработаны общие методы решения динамической задачи - метод гамильтониана пути реакции, метод кривизны траектории, квантовая многомерная динамика, квантовая теория переходного состояния. Главная идея динамических методов - выделить движение реагентов вдоль координаты реакции и учесть влияние всех других движений - и "ассистирующих", и тормозящих. Взаимодействие всех типов движения - вдоль координаты и прочих - рассматривается как "динамическое трение" и его расчет - одна из забот современной теории
Однако у теоретического могущества химии есть одна неприятная сторона Широкое и успешное применение методов квантовой химии, методов молекулярной динамики стимулирует прогрессирующую болезнь - уход от наукоемкого и дорогого эксперимента Это - объективная реальность и общая тенденция движения мировой химии (воз можно, не только химии)
Есть глубокое родство между теорией химических и ядерных реакций (причем не только в диффузионном режиме, где кинетические уравнения и их решения абсолютно тождественны) Химически реагирующая система в жидкости или твердом теле подобна реагирующим нуклонам в окружении среды - других нуклонов ядра. И здесь у химии положение выгодное - в ней есть простота, которая выражается в том, что работает только одно взаимодействие - кулоновское, с известной зависимостью энергии от расстояния Это утверждение фундаментального свойства оно следует из квантовой механики (законы которой также неоспоримо точны, как и законы классической механики) Но оно имеет и прямые экспериментальные доказательства Речь идет об экспериментальном зондировании атомных волновых функций, на которых стоит вся химия
Эксперимент этот очень прост: атомный пучок (Са или Сu) возбуждается поляризованным светом в состояния pz или dz2 , далее на этот пучок с ориентированными в пространстве орбиталями pz и dz2 направляется скрещенный пучок атомов Не, рассеяние которого детектируется, а затем по картине рассеяния восстанавливается рассеивающий потенциал Результат оказался очень наглядным профиль рассеяния точно воспроизводит форму атомных орбиталей
Конечно, можно сказать, что это банальный результат (в том смысле, что другой и не ожидался), но он дает глубокое понимание того, что в химии работает только кулоновский потенциал (часть которого - обменное взаимодействие - зависит от спина) Но если вспомнить, что атомные волновые функции получены на кончике пера из постулатов квантовой механики и уравнения Шредингера с центрально симметричным кулоновским потенциалом, то появляется осознание торжества человеческой мысли
Волшебство химии и ее очарование состоят в том, что из кулоновского потенциала рождается богатство химических связей (ионных, ковалентных, донорно-акцепторных, дативных, водородных, ван-дер-ваальсовых), химических частиц (атомы, карбены, ионы, молекулы, эксиплексы, ридберги, эксимеры, ван-дер-ваальсовы молекулы, комплексы, радикалы и др), состояний (основных, возбужденных, зарядовых, спиновых, орбитальных, различных по симметрии и т д), механизмов химических превращений и управляющих факторов (энергия, спин, фаза, орбитальная симметрия). В этом многообразии и богатстве химия всегда нова. Примером может служить открытие новых состояний молекул водорода (рис. 16).
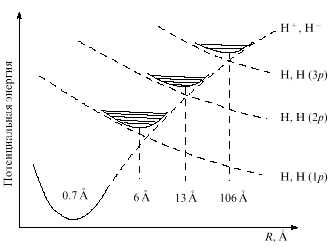 |
|
Им соответствуют минимумы адиабатических потенциальных кривых, расположенные в окрестностях точек пересечения связывающего терма Н+ + Н-(1s2) и отталкивательных термов H(ls) + Н(пр), где п = 1, 2, 3,.... Это не ридберговские молекулы, у которых "пухлая" электронная оболочка с главными квантовыми числами, достигающими сотен, а "нормальные" молекулы с равновесными межатомными расстояниями б, 13, 106 А и т.д. со своими колебательно-вращательными спектрами. Аналогичные молекулы могут существовать и в случае других атомов. Их можно обнаружить в низкотемпературной и разреженной плазме или в межзвездном гигантском химическом реакторе.