Скорость химической реакции. Определение.
Химические реакции протекают с разными скоростями. Из известных на сегодняшний день
реакций самая быстрая протекает в 1040 раз быстрее, чем самая медленная. Превращение
графита в алмаз в недрах Земли - очень медленная реакция. А взрыв смеси кислорода с
водородом происходит практически мгновенно.
Как сравнить скорости реакций количественно?
Скорость - это изменение некоторой величины во времени.
Рассмотрим реакцию:
H2 + I2 = 2HI
Попробуем определить скорость этой реакции по расходованию реагентов в единицу времени. Например, так:
v(H2) = m(H2)/Dt,
v(I2) = m(I2)/Dt
где v - скорость реакции, m
- убыль массы соответствующего реагента,
Dt - отрезок времени.
Но v(H2) не равно v(I2).
Ведь массы водорода и иода, прореагировавших в единицу времени, не равны.
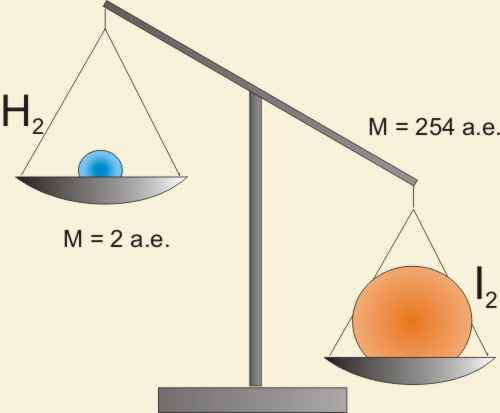
Реакция идет в мольном соотношении 1:1, а не в массовом! Попробуем по-другому:
v(H2) = n(H2)/Dt,
v(I2) = n(I2)/Dt
взяв вместо масс количества веществ.
v(H2) = v(I2)
Но если в первом случае мы возьмем убыль числа молей в единицу времени в 1 мл смеси,
а во втором - в 1 л смеси, то скорости снова не будут равны! Они зависят от объема. Если
проводить одну и ту же реакцию в маленькой пробирке и в большой бочке, то в пробирке
прореагирует меньшее количество вещества - просто потому, что там меньше реагента.
А если привести эти выражения к единице объема?
v(H2) = n(H2)/VDt
= Dc(H2)/Dt,
v(I2) = n(I2)/VDt=Dc(I2)/D t
где Dc изменения молярных концентраций соответствующих веществ.
Тогда vH2 = vI2 = v данной реакции!
Таким образом, конечное определение будет:
Скорость химической реакции - это изменение молярной концентрации одного
из участвующих в реакции веществ в единицу времени:
v = Dc/Dt [моль/литр*сек]
|
В принятом определении есть два нюанса! Хотите узнать, какие?
Приложения
| 






