


Метаболизм. Энергетика
Сохранение энергии на мембранах
 Наряду с макроэргическими соединениями
другим местом накопления химической энергии являются биологические мембраны. В
технике система, работающая за счет разделения электрических зарядов
непроводящим слоем, называется конденсатором. По принципу конденсатора
функционируют биомембраны, разделяющие подобно изолирующему слою заряженные
атомы и молекулы (ионы).
Наряду с макроэргическими соединениями
другим местом накопления химической энергии являются биологические мембраны. В
технике система, работающая за счет разделения электрических зарядов
непроводящим слоем, называется конденсатором. По принципу конденсатора
функционируют биомембраны, разделяющие подобно изолирующему слою заряженные
атомы и молекулы (ионы).
А. Электрохимический
градиент
В то время как искусственная липидная
мембрана для ионов практически не проницаема, биологические мембраны содержат
«ионные каналы», по которым отдельные ионы избирательно проникают через
мембрану (см. с. 220). Проницаемость и полярность мембраны зависят от
электрохимического градиента, т. е. от концентраций ионов по обе стороны
мембраны (концентрационного градиента) и от разности электрических
потенциалов между внутренней и внешней сторонами мембраны (мембранного
потенциала).
В состоянии покоя клеток мембранный
потенциал (потенциал покоя, см. с. 340) составляет от -0,05 до -0,09 В,
т.е. на внутренней стороне плазматической мембраны преобладает избыток
отрицательных зарядов. Потенциал покоя обеспечивается прежде всего катионами
Na+ и K+, а также органическими анионами и ионом
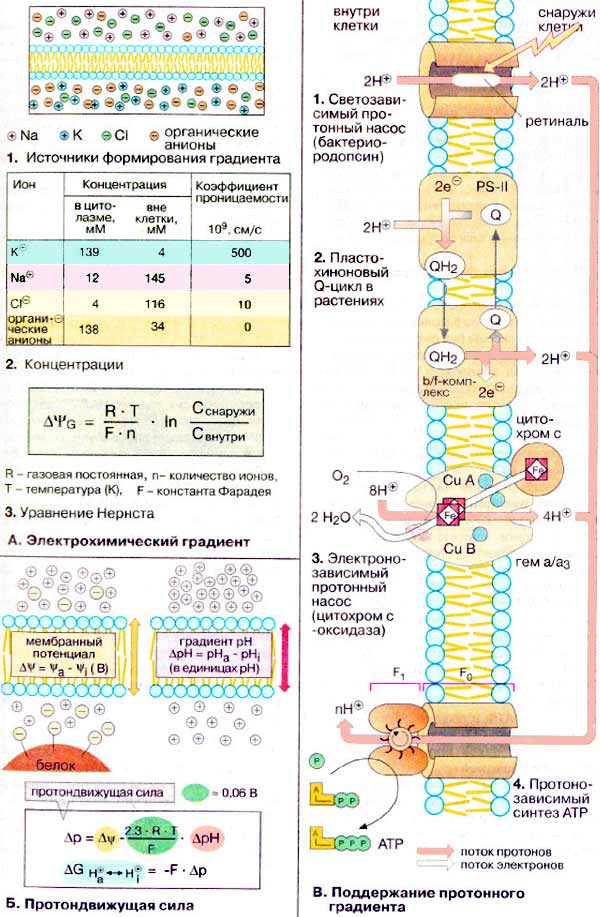
Cl- (1). Концентрации снаружи и внутри клетки и коэффициенты
проницаемости этих ионов приведены в таблице (2).
Распределение ионов между внешней средой и внутренним объемом
клетки описывается уравнением Нернста (3),
где ΔΨG — трансмембранный потенциал (в вольтах, В), т.е.
разность электрических потенциалов между двумя сторонами мембраны при отсутствии
транспорта ионов через мембрану (потенциал равновесия). Для одновалентных
ионов при 25оС множитель RT/Fn равен 0,026 В. Вместе с тем из таблицы
(2) следует, что для ионов К+ ΔΨG
примерно равно -0,09 В, т. е. величина того же порядка, что и потенциал покоя.
Для ионов Na+, напротив, ΔΨG = +0,07 В, т.е.
выше, чем потенциал покоя. Поэтому ионы Na+ поступают в клетку при
открытии Na+-канала (см. с. 340). Неравенство
концентраций ионов Na+ и К+ постоянно поддерживается Na+/K+-АТФ-азой
при расходовании АТФ (см. с. 222).
Б. Протондвижущая
сила
Ионы гидроксония («H+-ионы») также могут формировать
электрохимический градиент. Такой протонный градиент имеет решающее значение
для клеточного синтеза АТФ (см. с. 142). Как и в случае
других ионов, свободная энергия переноса протона (разность между электрохимическими
потенциалами протонов на двух сторонах мембраны) зависит от градиента концентрации,
т. е. от разности рН (ΔpH) по ту и другую стороны мембраны. Кроме
того, определенный вклад вносит и трансмембранный потенциал ΔΨ
(см. А). Обе эти величины формируют протондвижущую
силу Δp, являющуюся мерой работы ΔΨG , которую
может совершать H+-градиент. Таким образом, протонный градиент через
внутреннюю митохондриальную мембрану (см. с. 144) дает
примерно 24 кДж на моль переносимых ионов H+.
В. Поддержание протонного
градиента
Протонные градиенты формируются различными способами. Необычным
протонным насосом является бактериородопсин (1),
использующий энергию света (см. с. 130). При фотосинтезе
(см. с. 134) восстановленный пластохинон (QH2)
переносит протоны вместе с электронами через мембрану (Q-цикл, 2).
Образование протонного градиента в дыхательной цепи (см. с. 142)
также сопряжено с окислительно-восстановительным процессом. В комплексе III,
по-видимому, как и при фотосинтезе, за перенос прогона ответствен Q-цикл (не
показано). В цитохром с-оксидазе (комплекс IV, 3)
H+-транспорт сопряжен с электронным потоком от цитохрома с на О2.
В каждом из этих случаев протонный
градиент используется в синтезе АТФ АТФ-синтазой (4). АТФ-синтаза состоит
из двух компонентов: канала протонов (F0) и управляемого им белкового
комплекса (F1), который трансформирует энергию потока протонов через
мембрану в химическую энергию АТФ (см. с. 144).