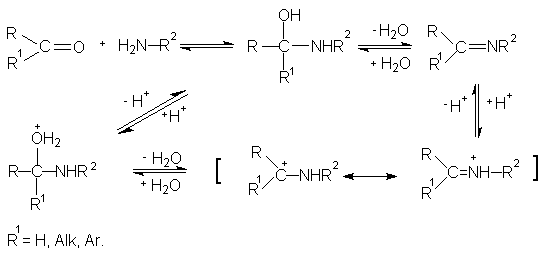
8.1. Бензилиденметиламин.
Альдегиды и кетоны реагируют с первичными аминами с образованием иминов (оснований Шиффа, азометинов).

Реакция протекает как нуклеофильное присоединение первичного амина по карбонильной группе с последующим элиминированием воды (кислотный катализ) через образование промежуточного иминиум-карбениевого иона. В данной методике взаимодействием метиламина с бензальдегидом получают бензилиденметиламин (R=C6H5, R`=H, R``=CH3). Аналогично осуществляется взаимодействие карбонильных соединений с гидроксиламином, гидразином,а также семикарбазидом. Продуктами реакции являются функциональные производные карбонильных соединений (оксимы, гидразоны и семикарбазоны).
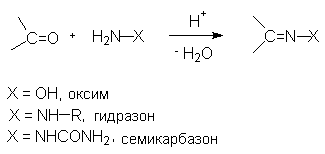
При проведении реакции альдегидов или кетонов с аммиаком или первичными аминами в присутствии восстановителей ( например, H2/Pd-C, Na[H3BCN] ) образуются первичные или вторичные амины ( восстановительное аминирование карбонильных соединений).
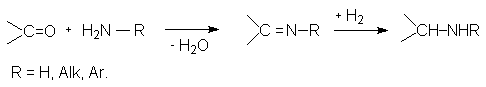
В реакции восстанавливается образующийся "in situ" имин.
Таким образом, бензилиденалкиламины являются промежуточными соединениями в препаративно направленном синтезе вторичных аминов из первичных. Вторая алкильная группа вводится при N-алкилировании бензилиденалкиламина диалкилсульфатом. Последующий гидролиз иминиевого соединения дает вторичный амин и бензальдегид.
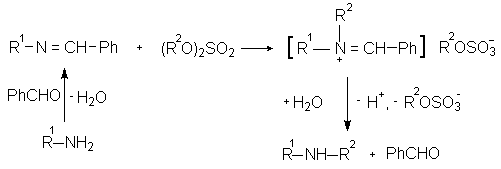
Методика.
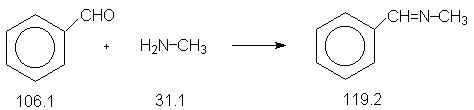
Константы исходных и синтезируемого соединения. Приведены формула, т.пл.оС, т.кип.оС, d420.
(C2H5)2O,-116.0, 34.5, 0.71;
C6H5CHO,-56.0, 179, 1.04;
CH3NH2,-93.5, -6.3,0.77;
C6H5CH=NCH3,-, 78/18 мм.
Проведение синтеза.
В трехгорлую колбу (100 мл), снабженную магнитной мешалкой, капельной воронкой, термометром и обратным холодильником (прибор 4) помещают 17.6 г(0.017 моля) 30 % раствора метиламина в воде. Из капельной воронки добавляют 15.9 г (0.015 моля) бензальдегида с такой скоростью, чтобы температура реакционной смеси не была выше 20оС. После окончания прибавления бензальдегида реакционную смесь перемешивают при комнатной температуре в течение 30 минут.
Обработка реакционной смеси.
В колбу добавляют 29 мл воды, органическую фазу
отделяют,а водную экстрагируют эфиром (3х25 мл).
Обьединенные органические слои сушат смесью
осушителей (Na2SO4+K2CO3).
Выделение : Растворитель отгоняют при атмосферном давлении, остаток перегоняют в вакууме. Получают 11.6 г (65 %) бензилиденметиламина в виде бесцветной жидкости с т.кип. 78-79оС(18 мм).
Примечание:~75 мл эфира могут быть собраны, очищены перегонкой и вновь использованы в синтезе.
Отходы, подлежащие обезвреживанию :~40 мл водной фазы, осушитель, предгон и остаток после перегонки.
Методы обработки реакционной смеси: 2.1, 2.2.
Выделение полученного продукта : 2.3, 3.4.
8.2. Бензоин.
Ароматические альдегиды при катализе цианид-ионом подвергаются димеризации с образованием a-гидроксикетонов. В случае бензальдегида образуется бензоин (Ar=C6H5).
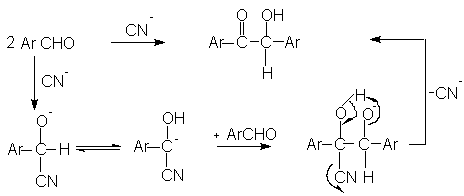
Бензоиновая конденсация обратима. Цианид-ион выполняет при этом тройную функцию: сначала он нуклеофильно присоединяется к карбонильной группе с образованием циангидрин-аниона, в котором происходит миграция протона от углерода к кислороду под влиянием –J эффекта циано-группы. Образующийся карбанион нуклеофильно присоединяется по карбонильной группе второй молекулы альдегида. После второй миграции протона цианид-ион выделяется из молекулы с образованием карбонильной группы бензоина. Циангидрин-карбанион представляет собой простой реагент для нуклеофильного ацилирования,т.е. перехода ацильной группы в карбанион. Обычно ацильная группа представляет собой электрофильный реагент, циангидрин-анион наоборот можно рассматривать в качестве синтетического эквивалента бензоиланиона.
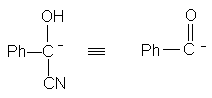
Этот принцип "переполяризации" реакционного центра играет важную роль. В этой связи следует напомнить о 1,3-дитианил-2-карбанионе (реагент Кори-Зеебаха) и силилциангидрин-карбанионе (реагент Хунига) как о эквивалентах ациланиону.
Циангидрин-карбанион является интермедиатом катализируемого цианид-ионом присоединения ароматических альдегидов к a,b-ненасыщенным карбонильным соединениям, в результате которого образуются 1,4-дикетоны (реакция Штеттера).
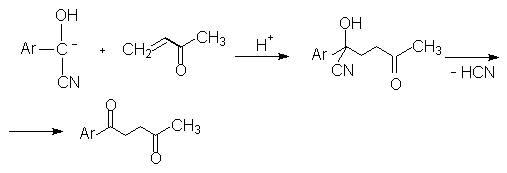
Методика.
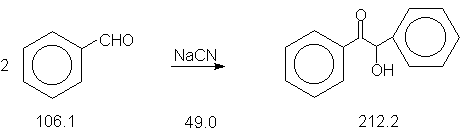
Константы исходных и синтезируемого соединения. Приведены формула, т.пл.оС, т.кип.оС.
C2H5OH, -117.0, 78.4,d420 0.79
;
C6H5CHO,-56.0, 179, d420
1.04;
NaCN,563.0, 1496.0 ;
C6H5COCH(OH)C6H5,135.
Выполнение синтеза.
В одногорлую колбу (100 мл) с обратным холодильником (прибор 1) помещают 8 г(0.075 моля) свежеперегнанного бензальдегида, 0.83 г (0.017 моля) цианида натрия (Осторожно! яд !) в 10 мл этанола и 10 мл воды. Реакционную смесь нагревают при кипении в течение 30 минут.
Обработка реакционной смеси.
Колбу оставляют на 1-2 часа в ледяной бане, выпавшие кристаллы отфильтровывают и промывают на фильтре небольшим количеством воды.
Очистка.
Перекристаллизовывают из ~ 40 мл этанола, выход 5.76 г(72 %), т.пл. 135оС. Разложение фильтрата, содержащего цианид: фильтрат подщелачивают NaOH или KOH (до рН ~ 9), смешивают с раствором FeSO4 и оставляют стоять некоторое время.
Примечание :~40 мл маточного раствора этанола могут быть собраны, очищены перегонкой и вновь использованы в синтезе.
Отходы, требующие обезвреживания :~ 30 мл маточного раствора, содержащего цианид-ион.
Методы обработки реакционной смеси и очистка полученного продукта: 3.2, 3.1.
8.3. Триэтилкарбинол (способ I).
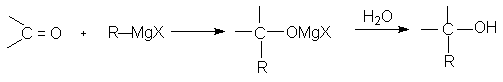
Присоединение алкил- или арилмагнийгалогенидов RMgХ( реактива Гриньяра, прототипа металлоорганического соединения) к альдегидам и кетонам является основным способом получения вторичных и третичных спиртов. Другими важными металлоорганическими соединениями являются RLi, R2CuLi, R2TiCl2. Взаимодействие a,b- ненасыщенных карбонильных соединений с литийорганическими соединениями проходит селективно как 1,2-присоединение, а с R2CuLi как 1,4-присоединение. С магнийорганическими соединениями чаще всего образуется смесь продуктов (1,2- и 1,4-присоединение).
Алкил- и, соответственно, арилмагнийгалогениды RMgX получают взаимодействием алкил- и арилгалогенидов с магнием.
![]()
Реактивы Гриньяра легко гидролизуются, поэтому их получают и вводят в реакцию с карбонильными соединениями в абсолютных растворителях, чаще в эфире. Разложение продуктов реакции проводят при осторожном гидролизе разбавленными кислотами или раствором хлорида аммония (охлаждение ледяной водой !). Взаимодействие реактива Гриньяра с карбонильными соединениями протекает как нуклеофильное присоединение поляризованного атома углерода реактива Гриньяра ("замаскированный " карбанион) к электрофильному атому углерода карбонильной группы. Реакция протекает неоднозначно и находится в зависимости от структуры субстрата, среды и температуры реакции. Предполагается образование как четырехчленого переходного состояния с участием одной молекулы RMgX, так и шестичленного переходного состояния с участием двух молекул RMgX. Возможно также появление радикалов в качестве промежуточных частиц. Продуктом реакции является алкоголят магния, при гидролизе которого образуется спирт. В предлагаемой методике триэтилкарбинол получают присоединением этилмагнийбромида к диэтилкетону. Альтернативным методом получения триэтилкарбинола является взаимодействие эфира пропионовой кислоты с двумя молями этилмагнийбромида или реакция трех молей этилмагнийбромида с диэтилкарбонатом (8.4 ).
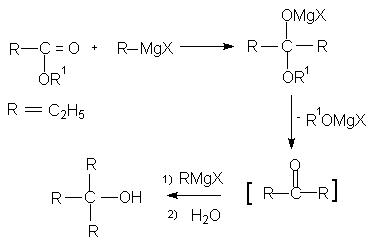
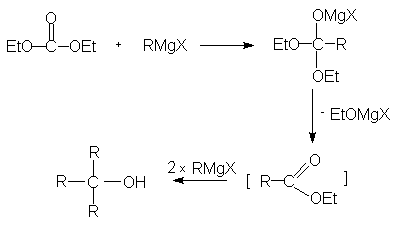
Реактив Гриньяра вступает в реакцию и с другими электрофилами. Так, при взаимодействии с диоксидом углерода образуются соответствующие карбоксилаты и далее в результате кислого гидролиза получают карбоновые кислоты (реакция карбоксилирования). При присоединении реактивов Гриньяра к нитрилам промежуточно образуются кетимины, которые могут быть гидролизованы до кетонов.
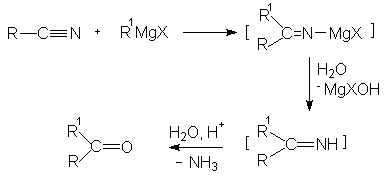
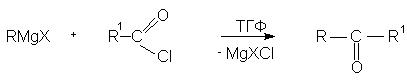
Взаимодействием реактивов Гриньяра с хлорангидридами кислот при низкой температуре в растворе тетрагидрофурана получают кетоны.
Методика.
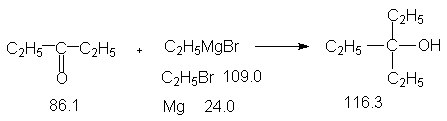
Константы исходных и синтезированного соединений. Приведены формула, т.пл.оС, т.кип.оС,d420.
(C2H5)2O,-116,0, 34.5, 0.71 ;
C2H5COC2H5, -42.0, 102.0,
0.85 ;
C2H5Br, -119.0, 38.0, 1.43 ;
Mg, 650.0, 1100.0;
HCOOH (~90 %), 8.4, 101.0 ;
(C2H5)3COH, -, 136.
Проведение синтеза.
В трехгорлую колбу (500 мл), снабженную мешалкой, капельной воронкой и обратным холодильником с хлоркальциевой трубкой (прибор 3) помещают 4.86 г(0.2 моля) магниевой стружки, добавляют в колбу ~6-7мл раствора 21.8 г(0.2 моля) бромистого этила в 100 мл абсолютного эфира. Реакционную смесь нагревают (без перемешивания) до начала реакции. Если реакция не начинается, добавляют 2-3 капли бромистого этилена при перемешивании и прибавляют оставшийся эфирный раствор бромистого этила с такой скоростью, чтобы поддерживать равномерное кипение эфира. После добавления всего раствора реакционную смесь нагревают при кипении в течение 30 минут. К реактиву Гриньяра прибавляют по каплям 13.8 г(0.16 моля) пентанона-3 в 25 мл абс. эфира, поддерживая слабое кипение эфира. Затем реакционную смесь нагревают при кипении еще 2 часа.
Обработка реакционной смеси.
Реакционную смесь при охлаждении ледяной водой гидролизуют осторожным добавлением раствора 11.5 г (0.25 моля) муравьиной кислоты в 100 мл воды. Эфирный слой отделяют , а водный экстрагируют эфиром (2х25 мл). Обьединенные эфирные вытяжки встряхивают с разбавленным раствором гидрокарбоната натрия и сушат сульфатом магния. Выделенный эфир отгоняют с небольшим дефлегматором при нормальном давлении и затем перегоняют продукт. Получают 12.1 г (65 %) триэтилкарбинола в виде бесцветной жидкости с запахом камфары,т.кип. 136оС, nD20 1.4305.
Примечание: Около ~175 мл эфира отгоняют из реакционой смеси, очищают перегонкой и снова используют в синтезе.
Отходы безвредные :~ 100 мл водной фазы,~100 мл промывных вод (NaHCO3).
Отходы, требующие обезвреживания : осушитель, предгон и остаток после перегонки продукта.
Методы обработки реакционной смеси и очистка полученного продукта : 2.1, 2.2, 2.3, 3.4.
8.4. Триэтилкарбинол (способ II).
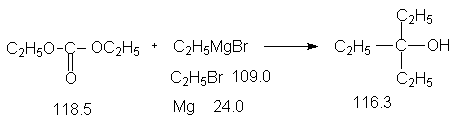
Константы исходных и синтезированного соединений. Приведены формула, т.пл.оС, т.кип.оС, d420.
Mg, 650.0, 1100.0 ;
C2H5Br, -119.0, 38.0, 1.43 ;
(C2H5)2O, -116.0, 34.5, 0.71;
HCOOH(~90%), 8.4, 101.0;
(C2H5)3COH, -,135, 0.82.
Проведение синтеза.
В прибор 1 помещают 9.1 г (0.37 г-ат) магниевой стружки и сразу добавляют порцию (~8 мл) раствора 41.0 г( 0.37 моля) бромистого этила в 80 мл абсолютного эфира. После начала реакции (нагревание, добавление каталитических количеств дибромэтана) при перемешивании прибавляют по каплям оставшийся раствор, поддерживая равномерное кипение эфира. Затем реакционную смесь нагревают на водяной бане в течение 30 минут. К полученному реактиву Гриньяра из капельной воронки прибавляют по каплям раствор 11.8 г(0.1 моля) диэтилкарбоната в 15 мл абс. эфира с такой скоростью, чтобы раствор слабо кипел. После окончания добавления реакционную смесь нагревают в течение 1 часа.
Обработка реакционной смеси.
Колбу охлаждают ледяной водой, осторожно добавляют раствор 23 г(0.5 моля) муравьиной кислоты в 100 мл ледяной воды. Эфирный слой отделяют, а водный экстрагируют эфиром (2х25 мл). Обьединенные эфирные вытяжки промывают 50 мл насыщенного водного раствора гидрокарбоната натрия и сушат прокаленным сульфатом натрия.
Выделение.
Осушитель отфильтровывают, эфир отгоняют при атмосферном давлении, а остаток перегоняют. Получают 9.3 г(80 %) триэтилкарбинола, т.кип. 135оС (760 мм), nD20 1.4290.
Примечание : Около ~150 мл эфира могут быть собраны, очищены перегонкой и вновь использованы в синтезе.
Отходы безвредные: ~ 100 мл водной фазы (разбавленая муравьиная кислота), ~50 мл промывных вод (NaHCO3).
Отходы, требующие обезвреживания: осушитель, предгон и остаток после перегонки продукта.
8.5. 1-Фенилциклогексен-1.
Третичные спирты, образующиеся при действии реактива Гриньяра на алифатические кетоны, подвергаются в сильно кислой среде дегидратации с образованием алкенов. Особенно легко элиминирование воды протекает в случае третичных бензиловых спиртов. Так, присоединение фенилмагнийбромида к циклогексанону и последующий гидролиз раствором хлорида амммония дает 1-фенилциклогексанол-1, который при обработке смесью H2SO4/CH3COOH превращается в фенилциклогексен-1.
Дегидратация, катализируемая кислотами, протекает по Е1 механизму через промежуточное образование третичного бензилкатиона, стабилизированного мезомерией.
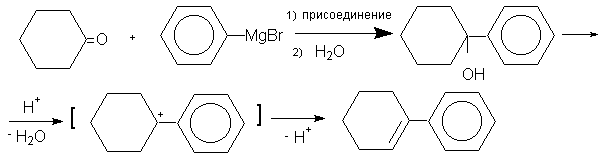
Методика.
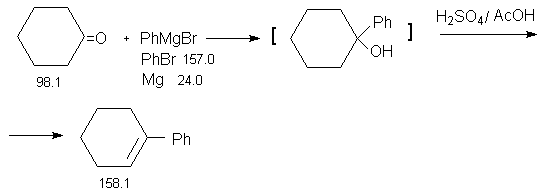
Константы исходных и синтезированного соединений. Приведены формула, т.пл.оС, т.кип.оС, d420.
Mg, 650.0, 1160.0;
C6H5Br, -31.0, 156.0, 1.49 ;
(C2H5)2O, -116.0, 34.5, 0.71 ;
циклогексанон,-16.4, 155.6, 0.95 ;
H2SO4, 10.3, 338.0;
CH3COOH, 16.6, 118.0, 1.05 ;
фенилциклогексен-1, -, 115оС(12 мм).
Проведение синтеза.
В трехгорлую колбу (250 мл) с обратным холодильником и хлоркальциевой трубкой, капельной воронкой с хлоркальциевой трубкой, магнитной мешалкой (прибор 3) помещают 3 г(0.125 моля) магниевой стружки и сразу прибавляют порцию в 5 мл от общего количества приготовленного раствора 19.6 г (0.125 моля) бромбензола в 50 мл абсолютного диэтилового эфира (Осторожно ! Огнеопасно !). Для инициирования реакции добавляют 1-2 капли сухого брома. Помутнение и самопроизвольное кипение реакционной смеси свидетельствуют о начале реакции. Далее прибавляют при перемешивании остальное количество раствора бромбензола в эфире, поддерживая равномерное кипение. После прибавления колбу нагревают еще в течение 1 часа. Затем при интенсивном перемешивании добавляют раствор 12.3 г циклогексанона в 10 мл абс. эфира (слабое кипение!). Для завершения реакции колбу нагревают в течение 30 минут.
Обработка рекционной смеси.
Колбу охлаждают ледяной водой. При перемешивании медленно (особенно вначале) прибавляют по каплям 100 мл насыщенного, охлажденного до 0оС, раствора хлорида аммония. Образуется два слоя, эфирный слой отделяют, а водный экстрагируют эфиром (2х20 мл). Обьединенные эфирные вытяжки сушат сульфатом натрия. Осушитель отфильтровывают и растворитель отгоняют при атмосферном давлении, а остаток выдерживают в вакууме водоструйного насоса. К полученному желтому маслу при перемешивании (магнитная мешалка) добавляют смесь 5 мл конц. серной кислоты и 20 мл уксусной кислоты. Нагревают в течение 15 минут при 50оС , затем охлаждают и выливают порциями в смесь 80 мл эфира и 125 мл воды. Эфирный слой отделяют, промывают насыщенным водным роаствором гидрокарбоната натрия (3х30 мл) и высушивают сульфатом магния.
Выделение.
Осушитель отфильтровывают и эфир отгоняют при атмосферном давлении. Остаток перегоняют в вакууме. Выделяют 18.8 г(92 %) фенилциклогексена в виде бесцветной жидкости, т.тип. 115оС(12 мм), nD20 1.5665.
Примечание:~ 180 мл эфира могут быть собраны, очищены и вновь использованы в синтезе.
Отходы безвредные:~100 мл водной фазы (NH4Cl), ~150 мл водной фазы(разб. H2SO4, CH3COOH).
Отходы требующие обезвреживания: осушитель. Предгон и остаток после перегонки конечного продукта.
Отходы безвредные :~100 мл водной фазы (NH4Cl), ~150 мл водной фазы(разб. H2SO4, CH3COOH).
Отходы требующие обезвреживания : осушитель, предгон и остаток после перегонки конечного продукта.
Методы обработки реакционной смеси и выделение полученного продукта: 2.1, 2.2, 2.3, 3.2, 3.4.
8.6. Реакция Канниццаро с бензальдегидом.
Взаимодействие альдегидов,не содержащих атомов водорода в a-положении к карбонильной группе, с концентрированной едкой щелочью приводит к смеси (1:1) первичного спирта и соответствующей карбоновой кислоты ( точнее ее калиевой или натриевой соли). В этом процессе, названном реакцией Канниццаро, протекает реакция диспропорционирования или окисления-восстановления между двумя молекулами альдегида (ароматического альдегида или формальдегида).
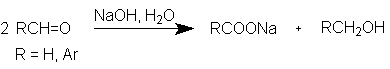
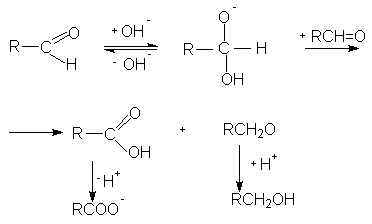
Начало реакции заключается в атаке иона гидроксила на углеродный атом карбонильной группы, полученный аддукт стабилизируется переходом гидрид-иона к карбонильному атому углерода второй молекулы альдегида и образованием карбоновой кислоты и алкоголята первичного спирта. Полученные кислота и анион алкоголята обмениваются протоном, при этом образуются спирт и анион кислоты, стабилизированный делокализацией своего заряда.
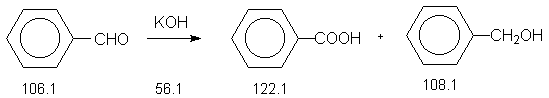
Так как формальдегид обладает более высокой карбонильной (электрофильной) активностью (и вместе с тем более высокой восстанавливающей способностью) чем ароматический альдегид, формальдегид может восстанавливать ароматические альдегиды в присутствии концентрированной едкой щелочи в ходе "перекрестной" реакции Канниццаро. В этом случае из бензойного альдегида образуется бензиловый спирт, а формальдегид окисляется в муравьиную кислоту.
![]()
Известно также внутримолекулярное диспропорционирование по реакции Канниццаро. Например, превращение глиоксаля в натриевую соль гликолевой кислоты происходит при добавлении раствора концентрированного гидроксида натрия.
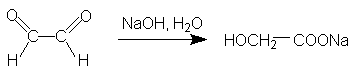
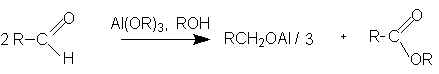
Если на альдегиды, не имеющие атомов водорода у a- углеродного атома, вместо концентрированной едкой щелочи действовать алкоголятом алюминия, то протекает диспропорционирование с образованием первичного спирта и эфира карбоновой кислоты (реакция Кляйзена-Тищенко).
Методика.
Константы исходных и синтезируемых соединений. Приведены формула, т.пл.оС. т.кип.оС,d420.
CH3OH, -94.0, 64.6, 0.79 ;
C6H5CHO, -56.0, 179.0, 1.04 ;
C6H5CH2OH, -15.3, 206.0, 1.045 ;
KOH, 410, 1327.0;
C6H5COOH, 122.
Проведение синтеза.
В трехгорлую колбу (250 мл), снабженную магнитной мешалкой, капельной воронкой и обратным холодильником (прибор 3) , помещают раствор 39.3 г(0.37 моля) бензальдегида в 75 мл метанола и нагревают смесь до 65оС. Затем нагревание убирают и прибавляют по каплям раствор 22.4 г(0.4 моля) гидроксида калия в 30 мл воды с такой скоростью, чтобы температура не поднималась выше 75оС (колбу охлаждают ледяной водой). После добавления щелочи реакционную смесь нагревают при 70-75оС в течение часа.
Обработка реакционной смеси и очистка продукта.
При охлаждении реакционной смеси ледяной водой выпадают кристаллы бензоата калия, которые отделяют фильтрованием. К маточному раствору добавляют 150 мл ледяной воды.
а) выделение бензилового спирта из маточного раствора: раствор экстрагируют эфиром (2х50 мл), обьединенные эфирные вытяжки сушат сульфатом магния. Эфир отгоняют при атмосферном давлении, остаток перегоняют в вакууме и получают 16.0 г(80 %) бензилового спирта, т.кип. 98оС(13 мм), nD20 1.5403.
б) выделение бензойной кислоты: бензоат калия растворяют в воде и подкисляют разбавленной соляной кислотой. Выпавшую бензойную кислоту отфильтровывают, промывают несколькими порциями холодной воды и прекристаллизовывают из горячей воды. Получают 9 г(40 %) бензойной кислоты,т.пл. 122оС.
Примечание:~100 мл эфира могут быть собраны, очищены перегонкой и вновь использованы в синтезе.
Отходы безвредные:~ 100 мл водной фазы, ~100 мл маточного раствора (при перекристаллизации бензойной кислоты).
Отходы. требующие утилизации:~250 мл маточного раствора (вода-метанол), осушитель, предгон и остаток после перегонки.