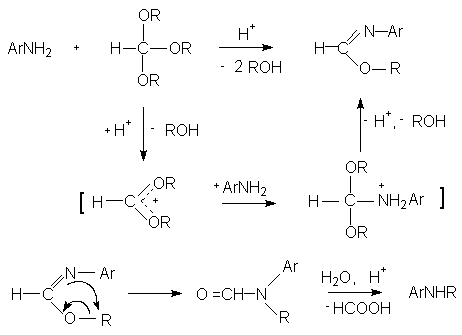
9.1.N-этил-мета-метилформанилид.
При взаимодействии первичных ароматических аминов с эфиром ортомуравьиной кислоты в присутствии сильных кислот ( например, серной кислоты) образуются О-алкил-N-арилформимидаты.
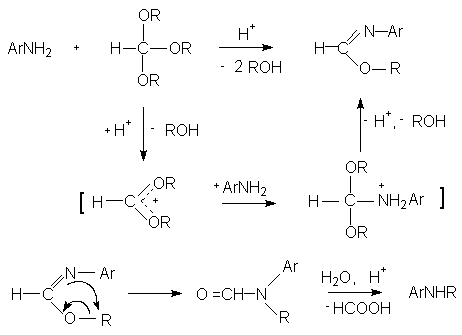
При высокой температуре О-алкил-N-арилформимидаты измеризуются в N-алкилформанилиды, т.е. происходит миграция алкильной группы от атома кислорода к атому азота ароматического амина. Эта перегруппировка имидоэфиров в амиды известна как перегруппировка Чапмана. Она интерпретируется как термически индуцируемый 1,3-N------O-сдвиг, протекающий через четырехцентровое переходное состояние. Движущей силой такой перегруппировки является образование амидной группы, стабилизированной изомерией. В приведенном синтезе N-этил-мета-метилформанилид гидролизуется 10%-ным раствором соляной кислоты до вторичного амина - N-этил-мета-толуидина и муравьиной кислоты. Вторичный амид идентифицируется как производное бензамида.
Перегруппировка Чапмана О-алкил-N-арилформамидов в N-алкилформанилиды с последующим гидролизом форманилида может служить методом получения вторичных алкилариламинов из первичных ароматических аминов, т.е. является селективным методом моноалкилирования первичных ароматических аминов.
Методика.
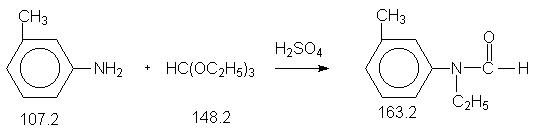
Константы исходных и синтезированного соединения. Приведены формула,т.пл.оС, т.кип.оС,d420.
3-CH3-C6H4NH2,-, 200, 0.99
;
H2SO4, 10.3, 338.0 ;
HC(OC2H5)3, -7.6, 146.0, 0.89 ;
3-C6H4-N(C2H5)CHO, -, 134-138оС(15
мм).
Проведение синтеза.
В трехгорлой колбе (150 мл) (прибор 9А) при интенсивном перемешивании нагревают смесь 13.4 г(0.125 моля) мета-толуидина, 27.8 г(0.188 моля) этилового эфира ортомуравьиной кислоты и 0.5 г конц. серной кислоты (тяга !). При температуре бани 105оС реакционная смесь начинает закипать, продолжают нагревание и этанол начинает отгоняться. В конце реакции температура в колбе достигает 175оС. Реакционную смесь выдерживают при этой температуре до прекращения отгонки этанола( должно отогнаться примерно 17 мл этилового спирта).
Выделение.
Реакционную смесь охлаждают до 60оС при комнатной температуре и перегоняют в вакууме. Первая фракция содержит около 5 мл этилового эфира ортомуравьиной кислоты (не вошедший в реакцию),т.кип. 146оС или 40оС(15 мм). При температуре 134-138оС (15 мм) выделяют 15.6 г(76%) N-этил-мета-метилфрманилида в виде светложелтой жидкости, nD20 1.5360.
Примечание: Полученный продукт является исходным соединением в синтезе N-этил-мета-толуидина. Примерно 17 мл этанола могут быть собраны и очищены перегонкой.
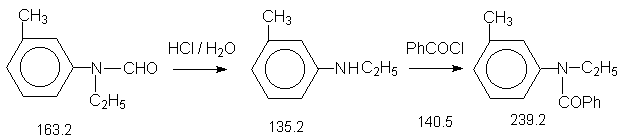
9.2. N-Этил-мета-толуидин.
Методика.
Константы исходных и синтезированного соединения. Приведены формула. т.пл.оС, т.кип.оС.
3-CH3-C6H4-N(C2H5)CHO, -,
134-138(15 мм) ;
HCl >25 %,-,110 ;
3-CH3-C6H4-NHC2H5, -,
96-97 (12 мм) ;
C6H5COCl, -0.5,197.1, d420
1.21 ;
3-CH3C6H4-N(C2H5)COC6H5,
69.
Проведение синтеза.
В трехгорлую колбу (100 мл) (прибор 3),снабженную механической мешалкой и обратным холодильником помещают 8.2г(0.05 моля) N-этил-мета-метилформанилида и 25 мл 10%-ной соляной кислоты. При интенсивном перемешивании полученную суспензию нагревают при кипении в течение 1 часа. При нагревании форманилид переходит в раствор.
Обработка реакционной смеси.
Реакционную смесь охлаждают ледяной водой и нейтрализуют карбонатом калия. Амин выделяется в виде бесцветного масла. Экстрагируют эфиром (2х30 мл). Обьединенные эфирные вытяжки промывают 30 мл ледяной воды и сушат прокаленным поташом.
Выделение.
Растворитель отгоняют при атмосферном давлении, остаток перегняют в вакууме. Выделяют 5.3 г( 78 %) N-этил-мета-толуидина, т.кип. 96-97оС(12 мм), nD20 1.5450.
9.3. N-Этил-N- бензоил-мета-толуидин.
В трехгорлую колбу (250 мл) (прибор 3) помещают 5.3 г(0.04 моля) амина, 5.63 г(0.04 моля) бензоилхлорида и 10 мл воды. При перемешивании прибавляют концентрированный раствор гидроксида калия до образования щелочной среды. При охлаждении ледяной водой образуются кристаллы амида. Осадок отделяют, промывают ледяной водой и высушивают в вакуум-эксикаторе. Получают 9 г(75 %) амида, т.пл. 65оС. Перекристаллизовывают из смеси этанол-вода (растворяют в небольшом количестве горячего этанола и добавляют воду до начала помутнения). Затем охлаждают ледяной водой, кристаллы отфильтровывают и сушат. Температура плавления полученного амида 69оС.
10. Реакции С-Н кислотных соединений.
10.1. Бензальацетон.
Альдегиды и кетоны, имеющие в ![]() -положении к карбонильной
группе CH3-, CH2- или CH-группы в условиях
основного катализа реагируют со второй
молекулой карбонильного соединения. При этом
возникает новая углерод-углеродная связь и
образуются
-положении к карбонильной
группе CH3-, CH2- или CH-группы в условиях
основного катализа реагируют со второй
молекулой карбонильного соединения. При этом
возникает новая углерод-углеродная связь и
образуются ![]() -гидроксикарбонильные
соединения (альдольное присоединение) или
альдольная конденсация.
-гидроксикарбонильные
соединения (альдольное присоединение) или
альдольная конденсация.
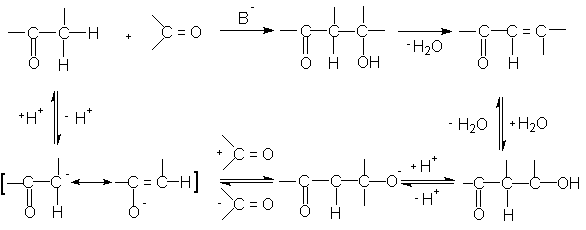
Водородные атомы, находящиеся у углорода соседнего с карбонильной группой, отличаются подвижностью и способны отщепляться в виде протонов в присутствии основных катализаторов. Их подвижность обьясняется электроноакцепторным влиянием карбонильной группы. Образующийся мезомерный енолят-анион быстро взаимодействует по типу нуклеофильного происоединения с карбонильной группой другой молекулы. Алкоголят, образующийся в результате димеризации, стабилизируется за счет переноса протона растворителя (вода, спирт). Во всех случаях конденсации генерированную енольную форму называют метиленовой компонентой, а реагирующее с ней карбонильное соединение – карбонильной компонентой.
Если в ![]() -положении
к карбонильной группе находится еще один атом
водорода, то возможна дегидратация
-положении
к карбонильной группе находится еще один атом
водорода, то возможна дегидратация ![]() -гидроксикарбонильного
соединения с образованием
-гидроксикарбонильного
соединения с образованием ![]() ,
,![]() - ненасыщенного соединения
(основной катализ по Е1-механизму). Этот процес с
называется кротоновой конденсацией.
- ненасыщенного соединения
(основной катализ по Е1-механизму). Этот процес с
называется кротоновой конденсацией.
Альдольная конденсация обратима на всех
стадиях. Обратная реакция (расщепление ![]() ,
,![]() -
ненасыщенного карбонильного соединения по С=С
связи с образованием метиленовой и карбонильной
компоненты) называется ретро-альдольной
конденсацией. Альдольная конденсация между
двумя различными карбонильными соединениями с
-
ненасыщенного карбонильного соединения по С=С
связи с образованием метиленовой и карбонильной
компоненты) называется ретро-альдольной
конденсацией. Альдольная конденсация между
двумя различными карбонильными соединениями с ![]() –СН- или
–СН- или ![]() -СН2-группами
(перекрестная альдольная конденсация, как
правило, приводит к смеси продуктов).
-СН2-группами
(перекрестная альдольная конденсация, как
правило, приводит к смеси продуктов).
Возможна направленная альдольная конденсация благодаря модификации функциональной группы (например, взаимодействие металлированных иминов с карбонильными соединениями, называемое альдольной конденсацией по Виттигу).
Если у одного из двух компонентов отсутствуют ![]() -водородные
атомы, то перекрестная альдольная конденсация
протекает региоселективно. Так, при
катализируемой основаниями альдольной
конденсации ацетона с одним молем бензальдегида,
образуется бензальацетон в качестве
единственного продукта. Альдоль не удается
выделить из-за его крайней неустойчивости.
Карбонильный атом углерода бензальдегида
является более сильным электрофилом по
сравнению с аналогичным атомом ацетона, имеющего
в молекуле два заместителя с +J -эффектом.
Самоконденсация ацетона также не происходит в
этих условиях.
-водородные
атомы, то перекрестная альдольная конденсация
протекает региоселективно. Так, при
катализируемой основаниями альдольной
конденсации ацетона с одним молем бензальдегида,
образуется бензальацетон в качестве
единственного продукта. Альдоль не удается
выделить из-за его крайней неустойчивости.
Карбонильный атом углерода бензальдегида
является более сильным электрофилом по
сравнению с аналогичным атомом ацетона, имеющего
в молекуле два заместителя с +J -эффектом.
Самоконденсация ацетона также не происходит в
этих условиях.
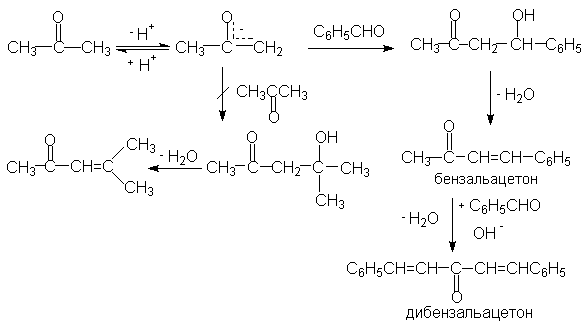
Бензальацетон может вступить в реакцию со
второй молекулой бензальдегида, образуя
дибензальацетон. Следовательно, если кетон имеет
водородные атомы при обоих атомах углерода,
расположенных в ![]() - положениях к карбонильной
группе, например, в случае ацетона, то могут
образовываться продукты моно- и диальдольной
конденсации. Для получения моноаддукта
необходимо ввести метиленовую компоненту в
2-3-кратном избытке.
- положениях к карбонильной
группе, например, в случае ацетона, то могут
образовываться продукты моно- и диальдольной
конденсации. Для получения моноаддукта
необходимо ввести метиленовую компоненту в
2-3-кратном избытке.
При проведении альдольно-кротоновой конденсации в кислой среде метиленовой компонентой является енол, а карбонильной – активированный в результате протонирования карбонильной группы альдегид или кетон. В этих условиях редко удается остановить реакцию на стадии образования соответствующего альдоля, так как он очень легко подвергается дегидратации.
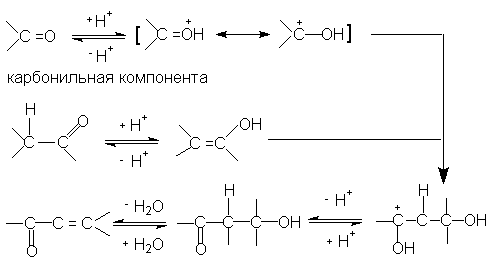
В случае несимметричных кетонов альдольные конденсации протекают по разным направлениям, в зависимости от применения кислого или основного катализа. Так, метилэтилкетон конденсируется с бензальдегидом при основном катализе по CH3 –группе (метильная группа является более кислой по сравнению с метиленовой). В условиях кислого катализа конденсация протекает по метиленовой группе,так как происходит преимущественное образование более замещенного енола.
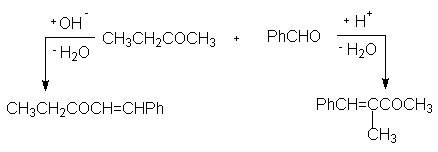
Методика.
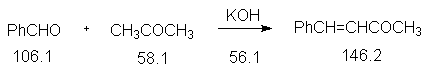
Константы исходных и синтезированного соединений. Приведены формула, т.пл.оС, т.кип.оС,d420.
C6H5CHO, -56.0,179.0, 1.04 ;
CH3COCH3, -94.9, 56.5, 0.79 ;
CH3OH, -94.0, 64.0, 0.79 ;
(C2H5)2O, -116.0, 34.5, 0.71 ;
CH3COOH, 16.6, 118,0, ;
C6H5CH=CHCOCH3, 41, 261.
Проведение синтеза.
В трехгорлую колбу (250 мл) ,снабженную механической мешалкой, капельной воронкой и термометром (прибор 4) помещают 13.3 г(0.125 моля) свежеперегнанного бензальдегида, 21.8г(0.375 моля) ацетона, 25 мл метанола и прибавляют по каплям 2.34г(0.006 моля) 15% раствора гидроксида калия, поддерживая температуру внутри прибора 20-25оС. Реакционную смесь перемешивают в течение 1 часа при комнатной температуре.
Обработка реакционной смеси.
Раствор нейтрализуют уксусной кислотой (по универсальному индикатору), разбавляют 150 мл воды и экстрагируют эфиром (2х50 мл). Обьединенные эфирные вытяжки промывают водой и высушивают над сульфатом натрия.
Выделение.
Осушитель отфильтровывают, растворитель отгоняют при атмосферном давлении. Остаток перегоняют в вакууме с воздушным холодильником. Получают 11.0г(60%) бензальацетона, т.кип. 140оС(16 мм). Вещество при стоянии или охлаждении ледяной водой кристаллизуется, т.пл. 41оС.
Примечание: Бензальацетон сильно раздражает кожу, поэтому при работе с ним необходимо соблюдать осторожность.
Примерно 100 мл эфира могут быть собраны и после повторной перегонки вновь использованы в синтезе.
Отходы безвредные : ~50 мл промывных вод.
Отходы, подлежащие утилизации : ~150 мл водной фазы, осушитель, предгон и остаток после перегонки.
Методы обработки реакционной смеси и выделение продукта: 2.1, 2.2, 2.3, 3.4.
10.2. Дибензальацетон.
Методика.
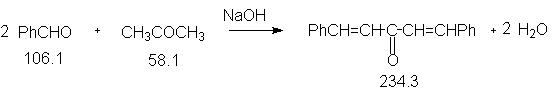
Константы исходных и синтезированного соединений. Приведены формула, т.пл.оС, т.кип.оС, d420.
C6H5CHO, -56.0,179.0, 1.04 ;
CH3COCH3, -94.9, 56.5, 0.79 ;
C2H5OH, -, 78, 0.79 ;
CH3COOC2H5, -, 77.0, 0.9 ;
C6H5CH=CH-CO-CH=CHC6H5,111.
Проведение синтеза.
В трехгорлую колбу (100 мл) (прибор 4) помещают раствор 3 г гидроксида натрия в 30 мл воды и 24 мл этилового спирта. При интенсивном перемешивании последовательно прибавляют 1,6 г (0.015 моля) свежеперегнаного бензальдегида и 0.45 г (0.0075 моля) ацетона, поддерживая температуру реакционной смеси 20-25оС. Реакционную смсеь перемешивают в течение 20 минут и прибавляют вторую порцию бензальдегида (1.6 г) и ацетона (0.45 г). Реакционную массу перемешивают в течение 30 минут.
Обработка реакционной смеси.
Осадок отфильтровывают, промывают ледяной водой и сушат на воздухе. После перекристаллизации получают 2.7 г(77 %) дибензальацетона, т.пл. 111оС.
Методы обработки реакционной смеси и выделение продукта: 3.2, 3.1.