9.1. Особенности строения и прочность связи Cl-O в оксоанионах.
В водных растворах оксокислоты хлора
диссоциируют, многие из них известны только в
растворе, поэтому, за исключением слабой HClO,
имеет смысл сравнивать строение (cтроение
газообразной HClO4установлено
электронографически: атомы кислорода
расположены в вершинах искаженного тетраэдра) и
свойства оксоанионов. В ряду HClO-HClO2--HClO3-HClO4
пространственное строение анионов изменяется
(табл.7) от линейного в случае ![]() до тетраэдрического в
до тетраэдрического в ![]() .
.
Таблица 7.Строение и свойства оксокислот хлора.
Формула кислоты |
HClO |
HClO2 |
HClO3 |
HClO4 |
| Длина связи Cl-O, |
1.69 |
1.64 |
1.57 |
1.45 |
| Углы |
|
|
|
|
| Eсвязи Cl-O, кДж/моль | 209.0 |
244.5 |
243.7 |
363 |
| рКa 25оС | 7.5 |
2.0 |
-1.2 |
-10 |
| Ео, B |
1.63 |
1.63 |
1.47 |
1.34 |
Следует отметить уменьшение межатомного
расстояния и увеличение энергии связи Cl-O в
анионах по мере увеличения в них числа атомов
кислорода. С позиции метода МО ЛКАО это связано с
увеличением числа электронов на связывающих
молекулярных орбиталях. С точки зрения метода
валентных связей (МВС), повышение прочности связи
Cl-O в ряду HClO-![]() может быть связано с увеличением связывания за
счет вакантных
может быть связано с увеличением связывания за
счет вакантных ![]() ,
, ![]() -орбиталей хлора и
электронов 2рх - и 2рy-орбиталей
кислорода, не участвующих в образовании
-орбиталей хлора и
электронов 2рх - и 2рy-орбиталей
кислорода, не участвующих в образовании ![]() -связей.
-связей.
9.2. Кислотные свойства. Индукционный эффект.
Из сопоставления величин рКa, приведенных в табл.7, следует, что легкость отщепления протона в оксокислотах уменьшается в ряду HClO4>HClO3>HClO2>HClO. Правила, характеризующие силу оксокислот, сформулированы Л.Полингом. Первое правило: величина первой константы диссоциации оксокислот (HO)nXOm определяется числом m концевых, негидроксильных атомов кислорода. Величину константы диссоциации pK1 = = -lgK1 для кислот (HO)nXOm можно оценить по уравнению рК1 = 8-5m. Это правило качественно объясняют так называемым индукционным эффектом. Индукционный эффект заключается в том, что более электроотрицательный концевой (негидроксильный) атом кислорода оттягивает на себя электронную плотность от атома хлора. Атом хлора с увеличенным положительным зарядом, в свою очередь, оттягивает электроны от атома кислорода гидроксильной группы. Таким образом, концевой атом кислорода понижает электронную плотность на связи Н-О, ослабляет ее и, тем самым, увеличивает легкость отщепления протона молекулами воды.
По мере перехода от HClO к HClO4 число концевых атомов кислорода и индукционный эффект увеличиваются, а сила кислот, соответственно, возрастает.
Второе правило Полинга касается величин констант диссоциации многоосновных кислот (HO)nXOm, где n>1: последовательные константы диссоциации К1, К2, К3, ј находятся в отношении 1: 10-5: 10-10. Это правило является эмпирическим, а уменьшение величин констант диссоциации обусловлено увеличением заряда аниона.
9.3. Стабильность оксокислот хлора и их солей.
Большинство оксокислот галогенов существуют только в водных растворах. Химические свойства кислот и их солей определяются стабильностью, или устойчивостью, анионов в кислых, нейтральных и щелочных средах.
Существуют два подхода к определению стабильности - термодинамический и кинетический. Соединение называют термодинамически устойчивым, если оно самопроизвольно не может превратиться в другие соединения. Это определение основано на законах термодинамики и относится к равновесию соединения с продуктами его распада или превращения. Термодинамический подход связан с представлением о начале и конце реакции. Он определяет возможную степень превращения исходных веществ в конечные, то есть константу равновесия Кравн.. В свою очередь, величина Кравн. связана с различием энергий Гиббса конечных и исходных веществ уравнением:
![]()
Чем меньше разница ![]() rGo,
тем больше Кравн, а, следовательно,
соединение термодинамически менее стабильно
(устойчиво) по отношению к продуктам распада.
rGo,
тем больше Кравн, а, следовательно,
соединение термодинамически менее стабильно
(устойчиво) по отношению к продуктам распада.
Соединение считается кинетически устойчивым, если оно не изменяется во времени. Кинетический подход связан с описанием скорости установления термодинамического равновесия, то есть с механизмом реакций. Если время существования соединения, то есть время превращения его в конечные соединения, достаточно велико, например, больше времени, которое необходимо для его идентификации с помощью тех или иных приборов, можно говорить о кинетической устойчивости данного соединения.
Когда речь идет о равновесии, то можно использовать термин термодинамическая стабильность, или просто стабильность. Для характеристики кинетической устойчивости используется термин инертность, а для кинетической неустойчивости - термин лабильность.
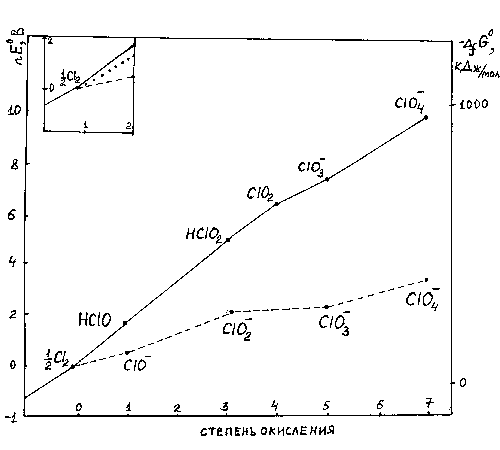
Рис.6. Диаграмма окислительных состояний хлора
при рН=0 (сплошная линия) и рН=14 (пунктирная
линия). Точками указан стандартный потенциал Ео=
1.23 В системы О2+4H++4![]() =2H2O.
=2H2O.
В растворах взаимное превращение оксокислот
хлора сопровождается изменением степени
окисления (СО) атома хлора. Поэтому
стабильность и окислительные (см.11.4)
свойства оксокислот хлора удобно обсудить,
используя диаграмму окислительных состояний
(рис.6) (диаграммы ВЭ-СО)(cтандартные окислительные
потенциалы Ео даются относительно
потенциала процесса H++![]() = 1/2H2. Методика построения
диаграмм ВЭ-СО и их использоваие описаны в 4-м
выпуске методического пособия по неорганической
химии для студентов 1-го курса. М., МГУ, 1993, с.24-30.),
предложенную Фростом (A.Frost. Oxidation Potеntial-Free Energy
Diagrams. J.Am.Chem.Soc. 1951. V.73. P.2680-2682)
= 1/2H2. Методика построения
диаграмм ВЭ-СО и их использоваие описаны в 4-м
выпуске методического пособия по неорганической
химии для студентов 1-го курса. М., МГУ, 1993, с.24-30.),
предложенную Фростом (A.Frost. Oxidation Potеntial-Free Energy
Diagrams. J.Am.Chem.Soc. 1951. V.73. P.2680-2682)
Диаграмма окислительных состояний (ОС) хлора
(рис.6) представляет графическую зависимость
вольт-эквивалента ВЭ = nEo, где Eо
- стандартный потенциал (В), n - количество (в
молях) электронов, пары частиц, например, HClOп 1/2Cl2
, от степени окисления. Величина nEo пропорциональна
стандартной энергии Гиббса ![]() Go
реакции превращения частиц HClO в Cl2 :
Go
реакции превращения частиц HClO в Cl2 : ![]() Go = -nEoF, где F =
96500 кал/моль - число Фарадея. Исходя из этого
диаграмму ВЭ-СО можно рассматривать как
зависимость стандартной энергии образования
Go = -nEoF, где F =
96500 кал/моль - число Фарадея. Исходя из этого
диаграмму ВЭ-СО можно рассматривать как
зависимость стандартной энергии образования ![]() fGo частиц от
степени окисления. Величины
fGo частиц от
степени окисления. Величины ![]() fGo
представлены на правой оси ординат рис.6.
fGo
представлены на правой оси ординат рис.6.
Термодинамически устойчивой к
диспропорционированию на диаграмме
окислительных состояний будет молекула (ион),
энергия Гиббса которой (правая ордината на рис.6)
лежит ниже линии, соединяющей энергии Гиббса
двух соседних форм. Например, при рН = 0 хлор (Cl2)
оказывается термодинамически стабильнее, чем
смесь ![]() +HClO. Термодинамически
это означает, что энергия Гиббса
+HClO. Термодинамически
это означает, что энергия Гиббса ![]() fG o( C l 2) меньше,
чем сумма
fG o( C l 2) меньше,
чем сумма ![]() fG o( C l -) и
fG o( C l -) и
![]() fG o( HC l O). Это
соответствует и известному факту, что равновесие
Cl2+H2O
fG o( HC l O). Это
соответствует и известному факту, что равновесие
Cl2+H2O ![]() H++
H++ ![]() + HClO при рН=0 смещено влево, так как Кравн.
= 4. 10-9.
+ HClO при рН=0 смещено влево, так как Кравн.
= 4. 10-9.
Сравним термодинамическую устойчивость оксокислот хлора при рН=0. Это эквивалентная оценка термодинамической возможности протекания процессов
3HClO = HClO3 + 2HCl (1),
3HClO2 = 2HClO3 + HCl (2),
4HClO3 = 3 HClO4 + HCl (3),
используя величины стандартных электродных потенциалов, приведенные в табл.7 и на схеме рис.7.
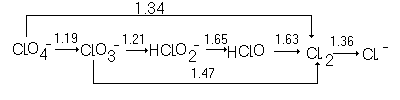
Рис.7. Потенциальная диаграмма (СВ), или диаграмма Латимера (рН=0).
Решение.
Термодинамическим условием протекания реакции
с точки зрения термодинамики является ![]() rG<0, то есть
rG<0, то есть ![]() . Для решения задачи рассчитаем
величины
. Для решения задачи рассчитаем
величины ![]() реакций (1)-(3)
реакций (1)-(3)
![]()
![]() ;
; ![]() .
.
Из диаграмм Латимера (рис.7) следует, что
![]()
![]()
![]()
![]()
![]()
![]()
Таким образом,
![]()
![]()
![]()
Во всех случаях Ео >О, следовательно, ![]() rGo<О, а
следовательно, и кислородные кислоты хлора HClO, HClO2,
HClO3 при рН=0 термодинамически нестабильны и
диспропорционируют по реакциям (1)-(3). Так как Е3>Е2>Е1,
то термодинамическая стабильность уменьшается в
ряду HClO - HClO2 - HClO3.
rGo<О, а
следовательно, и кислородные кислоты хлора HClO, HClO2,
HClO3 при рН=0 термодинамически нестабильны и
диспропорционируют по реакциям (1)-(3). Так как Е3>Е2>Е1,
то термодинамическая стабильность уменьшается в
ряду HClO - HClO2 - HClO3.
Аналогичным образом можно доказать и возможность протекания реакций
5HClO = 2Cl2 + HClO3 +2H2O (4)
7HClO3 = Cl2 + 5HClO4 + H2O (5).
Кроме того, потенциал восстановления кислорода
O2 + 4H+ + 4e = 2H2O (6)
(![]() при рН = 0 и
при рН = 0 и ![]() (см. рис.6)) меньше, чем
потенциалы реакций (1)-(5), поэтому возможно, что,
например, HClO будет окислять воду с выделением
(см. рис.6)) меньше, чем
потенциалы реакций (1)-(5), поэтому возможно, что,
например, HClO будет окислять воду с выделением
кислорода ( уравнение реакции (7) нетрудно
получить комбинированием реакций![]() , а расчет ее потенциала приведен
далее)
, а расчет ее потенциала приведен
далее)
HClO = HCl + 1/2O2 (7).
Из рис.6 следует, что при рН=0 наиболее устойчивыми формами являются HClO4 и Cl2,так как они оказываются конечными продуктами всех реакций диспропорционирования (1-5) в рассматриваемой системе.
В щелочной среде потенциал и энергии Гиббса полуреакций, включающих ионы водорода, уменьшаются (рис.6). Соли оксокислот поэтому оказываются стабильнее, чем сами кислоты. Конечными продуктами распада оказываются хлориды и перхлораты.
Рассмотрим кинетическую стабильность оксокислот и их солей, то есть скорость реакций (1-5, 7). Она определяется тремя факторами:
Факторы 1 и 2 повышают энергию активации и
замедляют скорость реакции (1-3) в ряду HClO>HClO2>![]() , так что наиболее
медленной оказывается реакция (3). Кинетически
наиболее лабильными (неустойчивыми) будут
кислоты HClO и HClO2, а наиболее
инертной - хлорноватая кислота HClO3. В
частности, получить в растворе хлорную кислоту HClO4
путем диспропорционирования HClO3 невозможно
именно по кинетическим причинам. Фактор 3
приводит к тому, что процессы (4,5,7) оказываются
заторможенными, так как гетерогенные реакции,
сопровождающиеся выделением хлора и кислорода,
протекают гораздо медленнее, чем гомогенные
реакции диспропорционирования.
, так что наиболее
медленной оказывается реакция (3). Кинетически
наиболее лабильными (неустойчивыми) будут
кислоты HClO и HClO2, а наиболее
инертной - хлорноватая кислота HClO3. В
частности, получить в растворе хлорную кислоту HClO4
путем диспропорционирования HClO3 невозможно
именно по кинетическим причинам. Фактор 3
приводит к тому, что процессы (4,5,7) оказываются
заторможенными, так как гетерогенные реакции,
сопровождающиеся выделением хлора и кислорода,
протекают гораздо медленнее, чем гомогенные
реакции диспропорционирования.
В целом, все оксокислоты хлора термодинамически и кинетически нестабильны. Соли оксокислот хлора, наоборот, термодинамически и кинетически более устойчивы. Это связано с тем, что твердые соли построены из ионов, электростатическое взаимодействие которых повышает энергию кристаллической решетки и, соответственно, стабильность.
9.4. Окислительная способность оксокислот хлора.
Окислительная способность оксокислот хлора связана с возможностью понижения степени окисления в анионе кислоты HXOn, n = 1,2,3,4. С термодинамической точки зрения закономерности изменения окислительной способности, как и стабильности, оксокислот хлора удобно проанализировать с помощью диаграммы окислительных состояний (рис.6) .
1.Все oксокислоты являются сильными окислителями, о чем свидетельствует положительный наклон линий, соединяющих вольт-эквиваленты (энергии Гиббса) окисленных и восстановленных форм на рис.6.
2. Их окислительная способность соответствует
следующей последовательности: Cl2 <HClO
![]() HClO2 >HClO3 > HClO4,
что отвечает наклонам линий для пар 1/2
HClO2 >HClO3 > HClO4,
что отвечает наклонам линий для пар 1/2![]() . Например, раствор соли NaClO
окисляет
. Например, раствор соли NaClO
окисляет ![]() до Br2
в кислой, нейтральной и щелочной средах:
до Br2
в кислой, нейтральной и щелочной средах:
NaClO + 2KBr + H2O = NaCl +Br2 +2KOH (в щелочной
среде происходит дальнейшее окисление Br2
до ![]() ).
).
C помощью NaClO3 ![]() окисляется только в кислой среде:
окисляется только в кислой среде:
NaClO3+ 6KBr +3H2SO4 = 3Br2 + NaCl + 3K2SO4 + 3Н2О.
3. С увеличением рН = -lg[H+] окислительная способность уменьшается. Например, для реакции
![]()
![]()
в соответствии с уравнением Нернста
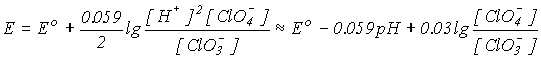 .
.
величина потенциала уменьшается от Ео = 1.02 В при рН = 0 до Ео= +0.37 при рН=14. Таким образом, окислительная способность солей ниже, чем соответствующих кислот.
С точки зрения кинетики для сопоставления окислительной способности кислот и оксоанионов хлора необходимо рассмотреть особенности механизма реакций. Изменение степени окисления может происходить двумя способами:
Оба варианта описания равноправны. С точки зрения метода молекулярных орбиталей (ММО) при этом важен факт перехода электронов с несвязывающих орбиталей на связывающие и наоборот (В случае комплексных соединений переходных металлов возможен переход электронов между несвязывающими орбиталями) . В любом случае для осуществления окислительно-восстановительной реакции сначала должен быть установлен контакт между частицами - канал, по которому может произойти переход электронов от восстановителя на свободные молекулярные орбитали окислителя.
В качестве примера присоединения атомной
группировки, сопровождающегося переносом
электронов (способ 2), рассмотрим механизм
окисления сульфит-иона ![]() хлорноватистой кислотой HClO. Результаты (K.D.Fogelman,
D.M.Walker, D.W.Margerum. Inorg.Chem, 1989, V.28, P.986-993) изучения
скорости реакции показывают, что первый
медленный этап - нуклеофильное (Нуклеофильные
(от латинского слова "нуклеус" - ядро)
частицы - частицы со свободной электронной парой,
стремящиеся к остову (ядру) другой частицы,
имеющей пустую орбиталь)присоединение к атому
хлора иона
хлорноватистой кислотой HClO. Результаты (K.D.Fogelman,
D.M.Walker, D.W.Margerum. Inorg.Chem, 1989, V.28, P.986-993) изучения
скорости реакции показывают, что первый
медленный этап - нуклеофильное (Нуклеофильные
(от латинского слова "нуклеус" - ядро)
частицы - частицы со свободной электронной парой,
стремящиеся к остову (ядру) другой частицы,
имеющей пустую орбиталь)присоединение к атому
хлора иона ![]() , в котором
имеются два электрона на разрыхляющей орбитали.
При этом образуется хлоросульфат-ион
, в котором
имеются два электрона на разрыхляющей орбитали.
При этом образуется хлоросульфат-ион![]() :
:
![]() (1)
(1)
В промежуточном комплексе (интермедиате) хлор
выступает как мостик между HO-- и ![]() . Вторая стадия - гидролиз
хлоросульфата - протекает быстро:
. Вторая стадия - гидролиз
хлоросульфата - протекает быстро:
![]() (2).
(2).
Скорость реакции (1) определяется доступностью
атома хлора для нуклеофильной атаки. В ряду Cl2 ![]() HClO < HClO2 < HClO3 < HClO4
увеличивается экранирование хлора атомами
кислорода, а значит, и уменьшается скорость
реакции, где указанные молекулы или ионы
выступают как окислители. Это интересный факт,
поскольку в рассматриваемом ряду окислительная
способность уменьшается как с точки зрения
термодинамики, так и с позиций кинетики.
HClO < HClO2 < HClO3 < HClO4
увеличивается экранирование хлора атомами
кислорода, а значит, и уменьшается скорость
реакции, где указанные молекулы или ионы
выступают как окислители. Это интересный факт,
поскольку в рассматриваемом ряду окислительная
способность уменьшается как с точки зрения
термодинамики, так и с позиций кинетики.
Следует также отметить, что скорость реакций, в которых оксоанионы действуют как окислители, ускоряется ионами водорода. Это связано с протонированием атомов кислорода в оксоанионе и ослаблением связи Cl-O, а также с увеличением электрофильности (электрофильная частица - частица с пустой орбиталью, которая стремится к остову другой частицы, имеющей свободную электронную пару) хлора по отношению к восстановителю, несущему электроны. Действительно, концентрированная HClO4, особенно в смеси с H2SO4, действует как сильный окислитель и взрывается в присутствии следов органических соединений (например, при попадании пыли).