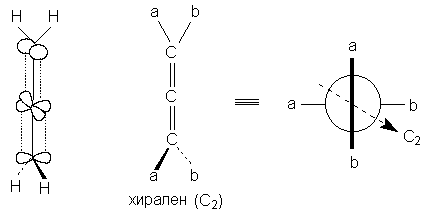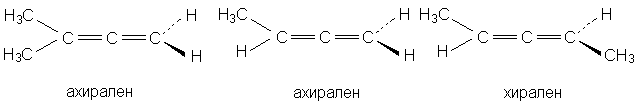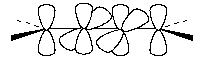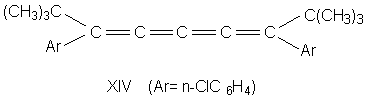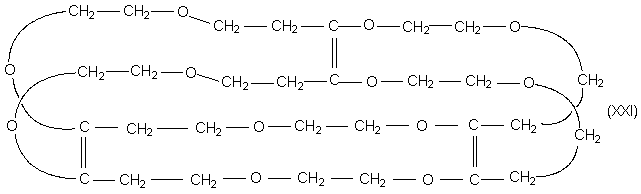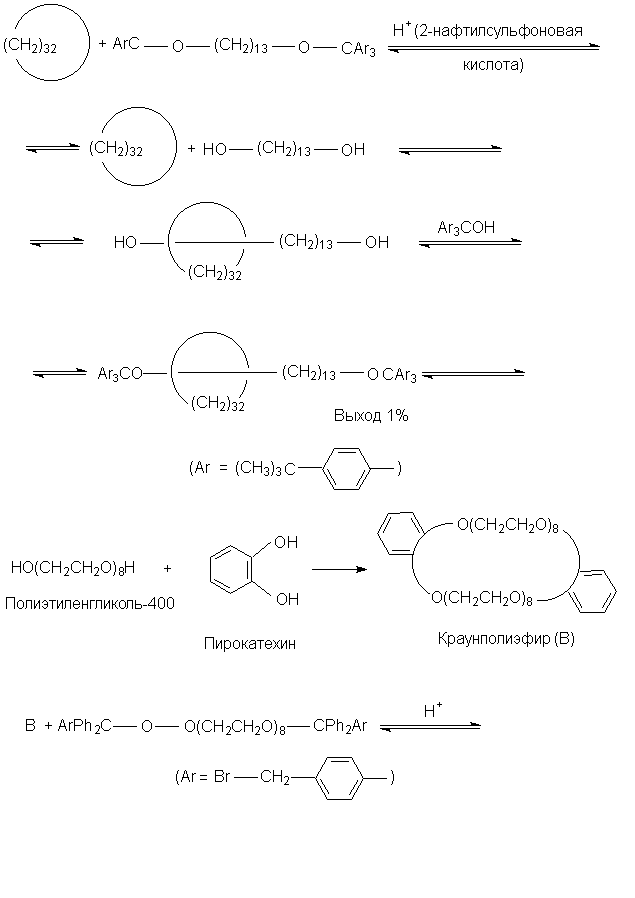|
Бутин К.П. Теоретическая стереохимия/ Органическая химия
8.2.2.б. Симметрийное определение
хиральности
Теперь рассмотрим вопрос: к каким точечным
группам симметрии должна принадлежать молекула,
чтобы она была хиральной? Другими словами, каким
должен быть характер диссимметрии молекулы, и
какие элементы симметрии обязательно должны
отсутствовать? Прежде всего очевидно, что
хиральна любая истинно асимметрическая
молекула, относящаяся к группе С1, не
имеющая никаких элементов симметрии, кроме
идентичности (и оси С1, т.к. С1  Е).
Очевидно, также, что молекулы, имеющие плоскость
симметрии (s ) или центр симметрии (i) ахиральны,
поскольку они состоят из двух одинаковых
"половинок" и в зеркальном отображении
левая и правая половинки преобразуются друг в
друга или без поворотов (при наличии плоскости),
или с поворотом на 1800 (при наличии центра
инверсии). Молекулы, имеющие
зеркально-поворотные оси (Sn) также
совмещаются со своим зеркальным отображением, и
поэтому ахиральны. Следовательно, хиральны
только молекулы, относящиеся к аксиальным
точечным группам Сn и Dn. Е).
Очевидно, также, что молекулы, имеющие плоскость
симметрии (s ) или центр симметрии (i) ахиральны,
поскольку они состоят из двух одинаковых
"половинок" и в зеркальном отображении
левая и правая половинки преобразуются друг в
друга или без поворотов (при наличии плоскости),
или с поворотом на 1800 (при наличии центра
инверсии). Молекулы, имеющие
зеркально-поворотные оси (Sn) также
совмещаются со своим зеркальным отображением, и
поэтому ахиральны. Следовательно, хиральны
только молекулы, относящиеся к аксиальным
точечным группам Сn и Dn.
Таким образом, можно сформулировать следующий
симметрийный критерий хиральности:
любая молекула, которая не имеет
несобственной оси вращения Sn хиральна.
Старое определение оптической изомерии, а
именно, "у молекулы не должно быть ни
плоскости, ни центра симметрии", недостаточно
точно. Поскольку S1  s и S2 s и S2  i, если у молекулы нет
несобственной оси вращения, то у нее не должно
быть ни s , ни i. Существуют молекулы, у которых нет
ни i, ни s , но есть ось Sn, и которые поэтому
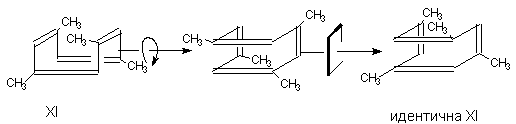
ахиральны. Примером является молекула
1,3,5,7-тетраметилциклооктатетраена (XI), у которой
нет ни плоскости, ни центра симметрии, но есть
зеркально-поворотная ось S4. Она оптически
неактивна. i, если у молекулы нет
несобственной оси вращения, то у нее не должно
быть ни s , ни i. Существуют молекулы, у которых нет
ни i, ни s , но есть ось Sn, и которые поэтому
ахиральны. Примером является молекула
1,3,5,7-тетраметилциклооктатетраена (XI), у которой
нет ни плоскости, ни центра симметрии, но есть
зеркально-поворотная ось S4. Она оптически
неактивна.
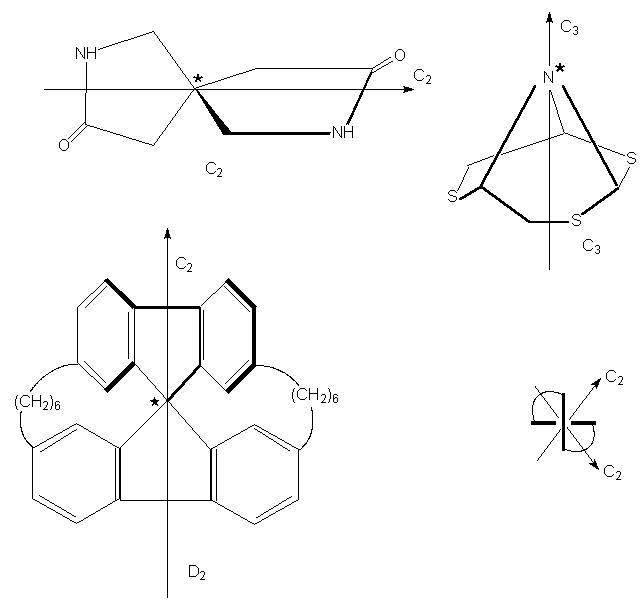
 Впервые доказательство справедливости данного
выше определения хиральных молекул получено при
исследовании изомерных четвертичных аммонийных
солей со спирановым атомом азота IV, V, VII и IX.
Изомеры IV и V асимметричны (группа C1), изомер
VII диссимметричен (группа D2). Поэтому эти
три изомера должны быть хиральными. И
действительно, они были получены в оптически
активной форме. Однако изомер VIII относится к
группе S4, т.е. ахирален, и получить его в
оптически активной форме нельзя.
8.2.2.в. Правила классификации молекул по
симметрии
Структура молекул органических соединений
бывает настолько сложной, что поиск возможных
элементов симметрии часто представляет собой
очень трудную задачу. Поэтому необходим
какой-либо разумный практически метод
последовательных действий при классификации
молекул по точечным группам симметрии. Ниже
описана схема метода, предложенного Ф.Коттоном в
1971 г.
1) Сначала необходимо определить, принадлежит
ли молекула к одной из следующих групп: (СҐ v (симметрия
конуса), DҐ h (симметрия цилиндра), Ih, Oh,
Td (тип 4, табл. 8.1). Эти группы условно назовем
"особые". Отметим, что к группе СҐ v или
DҐ h принадлежат только линейные молекулы,
например H-C C-Cl (СҐ v), H-C C-Cl (СҐ v), H-C C-H, Cl-C C-H, Cl-C C-Cl (DҐ h). и т.п. C-Cl (DҐ h). и т.п.
2) Если молекула не принадлежит к одной из
особых групп, необходимо поискать собственную
ось вращения Сn. Обнаружив такую ось,
переходим к операции (3). Если собственной
поворотной оси нет, необходимо искать центр
симметрии i или зеркальную плоскость s . Если у
молекулы окажется центр инверсии, она
принадлежит к точечной группе Сi, а если
окажется зеркальная плоскость, - к точечной
группе Сs. Если у молекулы нет элементов
симметрии (кроме Е), она относится к группе C1.
3) Далее находим главную ось Сn, т.е. ось
с наибольшим значением n. Определяем, есть ли
зеркально-поворотная ось S2n, совпадающая с
главной осью. Если она существует, а других
элементов, за исключением, возможно, i нет,
молекула принадлежит к одной из групп Sn,
где n - четное число. Если ось S2n есть, но
имеются и другие элементы, или если элемент S2n
отсутствует, необходимо перейти к операции (4).
4) Ищем набор из n осей второго порядка, лежащих в
плоскости, перпендикулярной Сn. Если такой
набор обнаружен, молекула принадлежит к одной из
групп Dn, Dnh или Dnd. Тогда
переходим к операции (5). Если же таких оcей нет,
молекула принадлежит к группе Сn, или Cnh,
или Cnv. Тогда переходим к операции (6).
5) Если у молекулы есть плоскость симметрии s h,
перпендикулярная главной оси, она принадлежит к
группе Dnh. Если такого элемента нет,
необходимо искать набор из n диагональных
плоскостей s d (т.е. плоскостей симметрии, в
которых находится главная ось, но не лежит ни
одна из перпендикулярных осей второго порядка).
Если отсутствуют и s d,и s h, молекула
принадлежит к группе Dn.
6) Если молекула имеет s h, она принадлежит
к точечной группе Cnh. Если s h
отсутствует, нужно искать набор из n плоскостей s v
(проходящих через главную ось). Наличие таких
плоскостей позволяет отнести молекулу к группе Сnv.
Если у молекулы нет ни s v, ни s h, она
относится к точечной группе Сn.
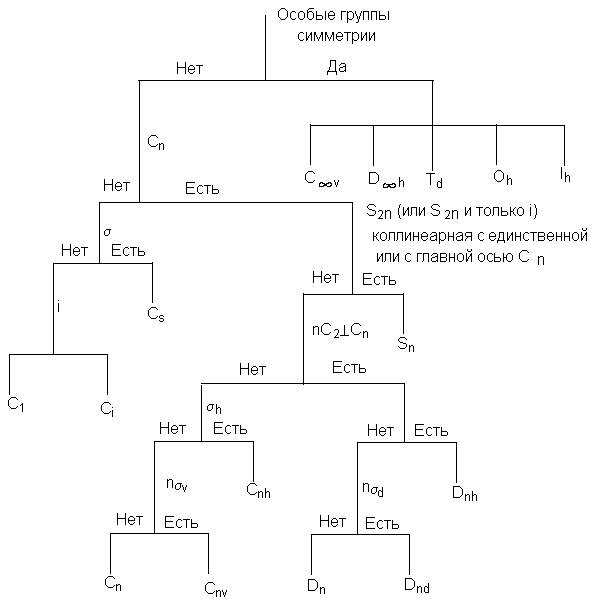
Изложенный метод иллюстрируется диаграммой,
приведенной на схеме 8.1.
8.2.2.г. Типы хиральности
Молекулы, содержащие тетраэдрический атом,
например, углерода с четырьмя разными
заместителями принадлежат к точечной группе С1.
Они асимметричны и центральный атом
называется асимметрическим атомом, как в
приведенном ниже примере a -бромпропионовой
кислоты (XII).
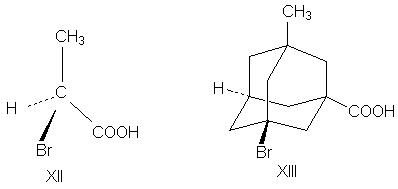
Схема 8.1
Адамантаны, у третичных атомов углерода
которых имеется четыре разных заместителя,
хиральны и оптически активны; например,
соединение XIII было разделено на энантиомеры. При
сравнении формул XII и XIII нетрудно видеть, что
симметрия обоих соединений очень похожа. Остов
адамантана можно представить как тетраэдр с
"изломанными ребрами", он имеет симметрию Td
которая переходит в C1, когда все четыре
заместителя у третичных атомов углерода разные.
У производного адамантана XIII нет
асимметрического атома углерода, как в a
-бромпропионовой кислоте, но есть центр,
находящийся внутри молекулы (центр тяжести
незамещенного адамантана). Асимметрический
центр - это частный случай более общего понятия
хиральный центр. Хиральный центр может иметь
не только асимметрические молекулы, но и
молекулы симметрии Cn или Dn. В
приведенных ниже примерах хиральный центр
помечен звездочкой.
Хиральный центр
является лишь одним из возможных элементов
хиральности. Молекулы, хиральность которых
обусловлена наличием центра хиральности,
безусловно, самые важные в органической химии.
Однако кроме центрального существуют еще и аксиальный,
планарный и спиральный типы хиральности.
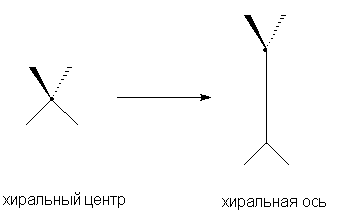
Аксиальной хиральностью обладают молекулы,
имеющие хиральную ось. Хиральную ось легко
получить, мысленно "растягивая" центр
хиральности:
Хиральную ось имеют такие классы молекул, как
аллены и дифенилы. В алленах центральный атом
углерода sp-типа имеет две
взаимно-перпендикулярные p-орбитали, каждая из
которых перекрывается с p-орбиталью соседнего
атома углерода, в результате чего остающиеся
связи концевых атомов углерода располагаются в
перпендикулярных плоскостях. Сам аллен хирален,
так как имеет зеркально-поворотную ось S4,
но несимметрично замещенные аллены типа
авС=С=Сав хиральны.
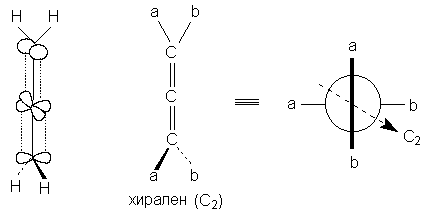
Аллены хиральны только в том случае, если оба
концевых атома углерода замещены несимметрично:
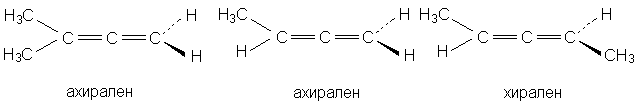
При любом нечетном числе кумулированных
двойных связей четыре концевые группы
располагаются уже не в разных, а в одной
плоскости, например, для 1,2,3-бутатриена:
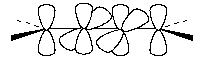
Такие молекулы ахиральны, но для них
наблюдается цис-транс-изомерия.
Так, соединение XIV было разделено на оптические
изомеры.
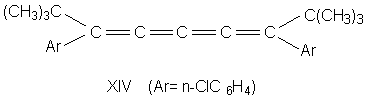
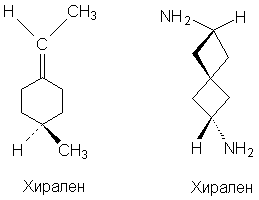
Если одну или обе двойные связи симметрично
замещенного аллена заменить на циклическую
систему, то полученные молекулы будут тоже
обладать аксиальной хиральностью, например:
В бифенилах, содержащих четыре объемистые
группы в орто-положениях, свободное вращение
вокруг центральной связи затруднено из-за
стерических препятствий, и поэтому два
бензольных кольца не лежат в одной плоскости. По
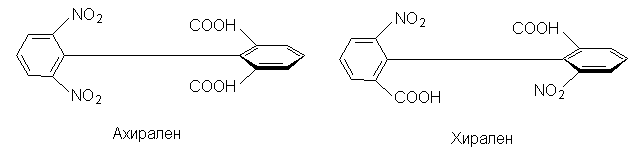
аналогии с алленами, если одно или оба бензольных
кольца замещены симметрично, молекула ахиральна;
хиральны же молекулы только с двумя
несимметрично замещенными кольцами, например:
Изомеры, которые можно разделить только
благодаря тому, что вращение вокруг простой
связи затруднено, называются атропоизомерами.
Иногда для предотвращения свободного вращения
в бифенилах достаточно трех и даже двух
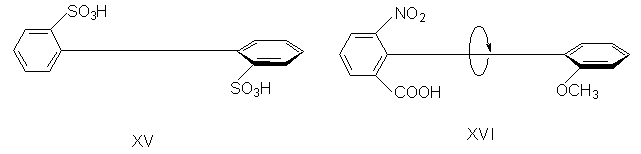
объемистых заместителей в орто-положениях. Так,
удалось разделить на энантиомеры
бифенил-2,2-дисульфокислоту (XV). В соединении XVI
свободное вращение полностью не заторможено, и,
хотя его можно получить в оптически активной
форме, при растворении в этаноле оно быстро
рацемизуется (наполовину за 9 мин. при 250).
Для некоторых хиральных молекул определяющим
структурным элементом является не центр, не ось,
а плоскость. Простейшую модель планарной
хиральности легко сконструировать из любой
плоской фигуры, не имеющей осей симметрии,
лежащих в этой плоскости, и отдельной точки вне
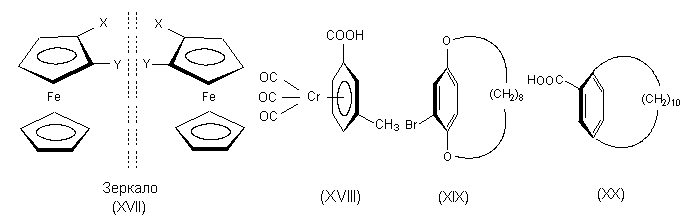
плоскости. Наиболее изучены планарно-хиральные
производные ферроцена (XVII). Другими примерами
являются ареновые комплексы хромтрикарбонила
(XVIII), а также соединения XIX и XX.
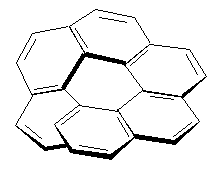
Спиральная хиральность обусловлена спиральной
формой молекулы. Спираль может быть закручена
влево или вправо, давая энантиомерные спирали.
Например, в гексагелицене одна часть молекулы
из-за пространственных препятствий вынуждена
располагаться над другой.
8.2.2.д. Хиральность макроциклических
молекул
Макроциклы, содержащие несколько десятков
атомов, соединенных в кольцо, способны
образовывать удивительные типы молекулярных
структур, обладающих левой или правой
спиральностью.
Например, в соединении XXI главная цепь имеет вид
ленты Мебиуса, которая должна существовать в
виде двух энантиомерных форм. Соединение XXI было
синтезировано и действительно оказалось
хиральным.
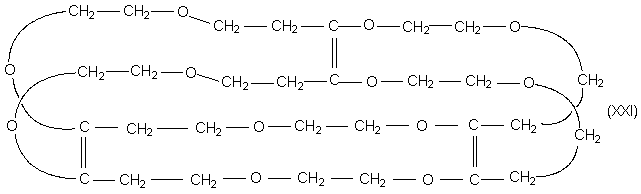
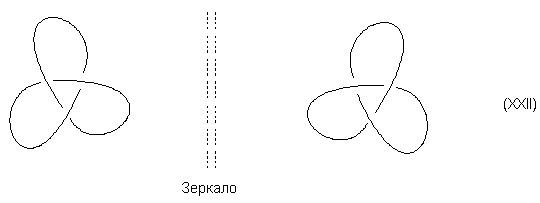
Циклы, состоящие из 60 или более членов могут
существовать в виде узлов (XXII), завязанных слева
направо или справа налево, и поэтому должны быть
хиральными.
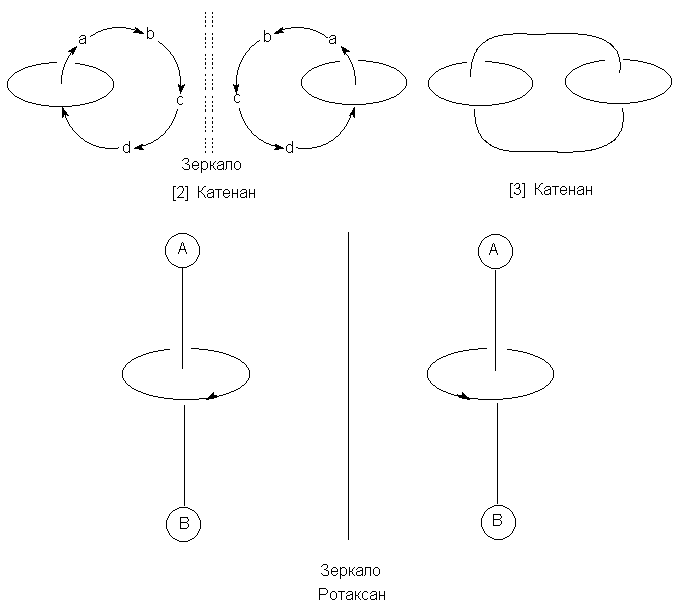
Хиральными могут быть также соответствующим
образом замещенные катенаны и ротаксаны. Эти
соединения состоят из двух или нескольких
самостоятельных частей, которые не связаны между
собой валентными связями, но тем не менее
удерживаются вместе. Катенаны построены из двух
или нескольких циклов, соединенных как звенья
цепи; в ротаксанах линейная молекула продета
сквозь циклическую молекулу и не может из нее
выскользнуть благодаря наличию объемных
концевых групп.
Катенаны и ротаксаны можно получить или
статистическим синтезом, или направленным
синтезом. Принцип статистического синтеза
пояснен следующей схемой.

Соединение А связывается по двум концам с
соединением Б в присутствии огромного избытка
макроциклического соединения В. До реакции с
молекулами Б какая-то часть молекул А должна
случайно оказаться продетой сквозь цикл В, и
поэтому наряду с продуктами Д и Е образуется
некоторое количество и ротаксана Г. Примеры
приведены ниже.
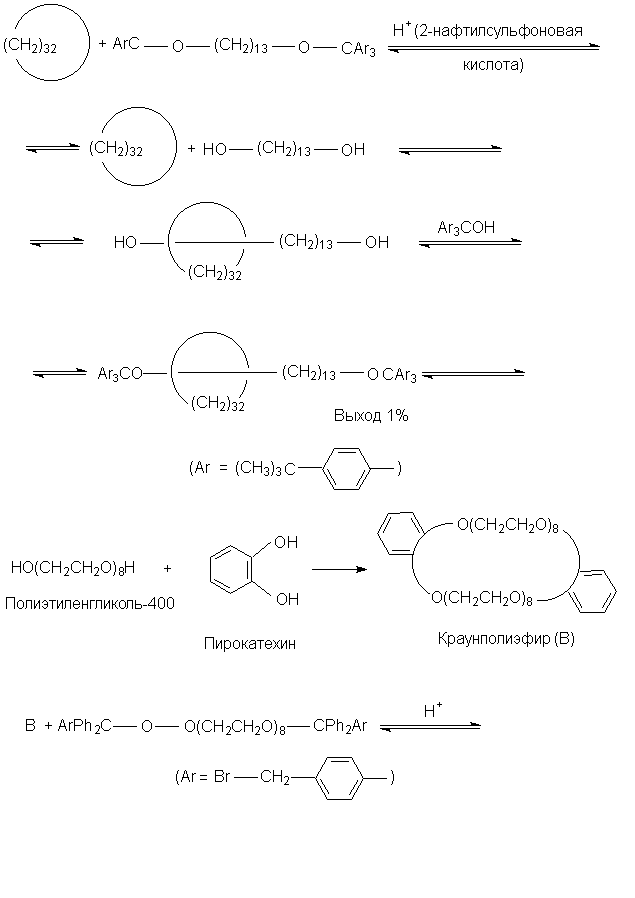
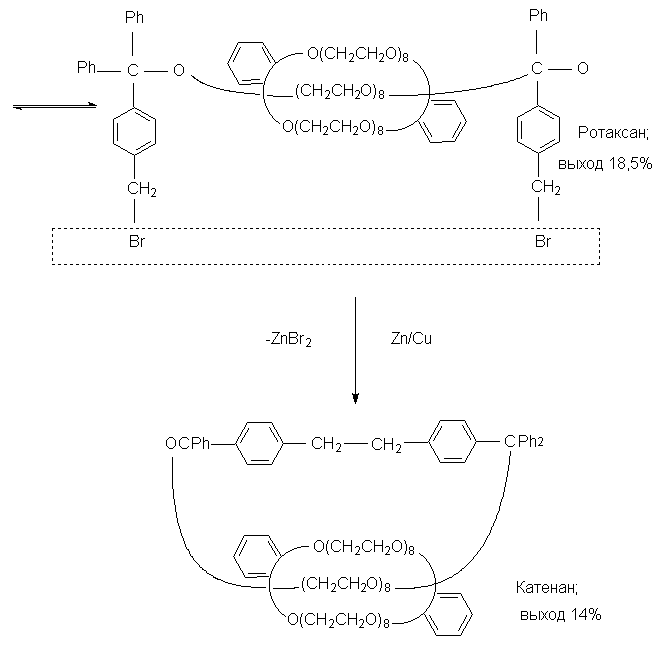
Хиральные катенаны и ротаксаны в настоящее
время еще не получены.
|